
|
|
麻酔と蘇生。 講義ノート: 簡単に言うと、最も重要なこと
目次
講義番号1.蘇生の概念 蘇生法は、体の活性化の問題を研究し、末期症状の予防のための原則、蘇生法、集中治療を開発する臨床医学の一分野です。 身体を活性化する実用的な方法は、「蘇生」の概念によって統合されています。 蘇生(ラテン語の「復活」または「アニメーション」から)は、身体の急激に損なわれた、または失われた重要な機能を回復し、それを終末状態および臨床的死から取り除くことを目的とした措置のシステムです。 効果的な蘇生法は、間接的な心臓マッサージと肺の人工換気です。 30 分以内に効果がなければ、生物学的死が確認されます。 集中治療は、重度の生命を脅かす状態を治療するために使用される一連の手段であり、適応症に応じて、静脈内注入、長期にわたる肺の人工換気、ペーシング、透析方法などを含む幅広い治療手段の使用を伴います. 重大な状態とは、臓器またはシステムの急性機能不全の結果として身体機能の完全性を維持することが不可能であり、薬物またはハードウェア機器の交換が必要になることです。 末期状態は、生と死の境界線にある状態であり、身体機能の可逆的な消滅であり、前苦悩、苦悩、臨床的死の段階を含みます。 臨床死は、血液循環と呼吸がなく、大脳皮質の活動が停止する末期状態ですが、代謝プロセスは維持されます。 臨床的死亡により、効果的な蘇生の可能性が残ります。 臨床死の持続時間は5分から6分です。 生物学的死は、蘇生が不可能な臓器や組織の生理学的プロセスの不可逆的な停止です。 それは多くの徴候の組み合わせによって確立されます:自発運動の欠如、大きな動脈の心臓と脈拍の収縮、呼吸、痛みを伴う刺激への反応、角膜反射、最大瞳孔拡張、および光に対する反応の欠如。 死の開始の信頼できる兆候は、体温が20°Cに低下し、死体の斑点と筋肉の硬直が出現することです。 講義番号2.集中治療における基本的な操作 主静脈(鎖骨下)の経皮的穿刺およびカテーテル挿入。 適応症:大量の輸液療法、非経口栄養、解毒療法、静脈内抗生物質療法、心臓のサウンディングとコントラスト、CVPの測定、ペースメーカーの埋め込み、末梢静脈のカテーテル法の不可能。 禁忌:血液凝固系の違反、穿刺およびカテーテル挿入部位での炎症性および化膿性プロセス、鎖骨の外傷、上大静脈症候群、パジェットシュレッター症候群。 穿刺およびカテーテル挿入用の器具および付属品: 穿刺針、プラスチック製カテーテルのセット、導体のセット、筋肉内注射用の 10 ml 注射器、はさみ、針ホルダー、外科用針および絹の結紮糸、絆創膏。 技術。 カテーテル法は、無菌および消毒の規則、オペレーターの手の治療、手術野、および滅菌材料でのラッピングに従って行われます。 患者の位置は、腕を体に近づけ、頭の襟を反対方向にして背中を水平にします。 局所麻酔が使用されます-0,5-1%ノボカイン溶液。 左鎖骨下静脈を穿刺する場合、胸管を損傷する危険性があるため、穿刺は右側で行うのが最適です。 穿刺点-鎖骨の2cm下の内側と中央45分の30の境界にあります。 針は、鎖骨に対して40°、胸鎖関節の上端の方向に鎖骨と第15肋骨の間の胸部の表面に対して20〜6°の角度でゆっくりと通過します。 針を通過するとき、注射器のプランジャーを定期的に締めて静脈に入るかどうかを判断し、針に沿ってノボカインを注入します。 静脈を刺すとき、時々失敗の感覚があります。 静脈に入った後、注射器を針から外し、カニューレを指で閉じます。 次に、導体を針を通して8〜XNUMX cmの長さに挿入し、針を取り外します。 適切な直径のカテーテルを導体に通し、導体と一緒にXNUMX〜XNUMX cm静脈に挿入した後、導体を慎重に取り外します。 カテーテルの正しい位置を確認するために、注射器を取り付けて2〜3mlの血液を注入した後、プラグを挿入するか、輸液療法を開始します。 カテーテルは絹の結紮糸で皮膚に固定されます。 これを行うには、皮膚から3〜5 mmのカテーテルに絆創膏のスリーブを作成し、その上にシルクを結び、カテーテルの耳に通して再び結びます。 カテーテルを固定した後、穿刺部位は無菌ステッカーで閉じられます。 合併症:鎖骨下動脈の穿刺、空気塞栓症、胸腔の穿刺、腕神経叢の損傷、胸部リンパ管の損傷、気管、甲状腺腫および甲状腺の損傷、穿刺部位の化膿。 1. 気管切開 適応症:腫瘍または異物による閉塞による喉頭および気管上部の閉塞、声帯の麻痺およびけいれん、喉頭の重度の腫れ、急性呼吸困難、嘔吐物の吸引、重度の胸部損傷における窒息の予防。 ツール:2つのメス、2つの解剖学的および外科用ピンセット、いくつかの止血クランプ、エレベーター、溝付きプローブ、2つの鈍いおよび1つの単歯の鋭いフック、TrousseauまたはDeschamps拡張器、持針器付きの外科用針。 機器 患者は仰向けになり、肩の下にローラーがあり、頭が後ろに倒されます。 患者が窒息状態にある場合、ローラーは気管を開く前の最後の瞬間にのみ配置されます。 局所浸潤麻酔は、アドレナリンを添加したノボカインの0,5〜1%溶液で行われます。 急性窒息では、麻酔なしで手術することが可能です。 識別ポイント:甲状軟骨の角度と輪状軟骨のアーチの結節。 皮膚、皮下組織、および表在筋膜の切開は、甲状軟骨の下端から首の正中線に沿って頸部ノッチまで行われます。 首の正中皮静脈が引っ込められるか結紮され、白い線が見つかります。それに沿って筋肉が鈍く押し離され、甲状腺の峡部が露出します。 切開の端をトルソー拡張器で離し、結紮を傷の端に適用し、気管切開チューブを注意深く挿入して、その端が気管の内腔に入るようにします。 外科的創傷は縫合されます。 チューブは、事前にチューブシールドに結び付けられたガーゼスプリントで患者の首に固定されています。 インナーチューブをアウターチューブに挿入します。 2. 円錐切除 患者は肩甲骨のレベルで横方向のローラーで背中に置かれます。 患者の頭は後ろに傾いています。 首の前面の皮膚を消毒液で処理した後、喉頭を指で甲状軟骨の側面に固定し、円錐形の靭帯がある甲状軟骨と輪状軟骨の間の隙間を感じた。 先の尖ったメスによる局所浸潤麻酔下で、長さ約 2 cm の横方向の皮膚切開を行い、円錐形の靭帯を触って切開または穿孔します。 適切な直径の任意の気管切開カニューレを、形成された穴に挿入し、首の周りにガーゼ ストリップで固定します。 カニューレがない場合は、適切な直径と長さのゴムまたはプラスチックチューブに置き換えることができます。 このチューブが気管に滑り込むのを防ぐために、その外側の端を端から2 cmの距離で横に突き刺し、ガーゼストリップで固定します。 Conicotome は、小径の金属製気管切開カニューレで、内部に貫通マンドレルが付いています。 円錐形の靭帯上の皮膚を切開した後、コニコトームで穴を開け、マンドレルを取り外し、カニューレを気管への空気の自由な流れを確保する位置に配置して固定します。 極端な場合、喉頭への入り口の閉塞と気道の急激な違反により、気管のレベルより下の正中線に沿って、内径1〜2 mmの2〜2,5本の太い針を気管に注入することで回復できます。甲状軟骨。 針は気管軸に対して鋭角で、時には局所麻酔なしで、1-1,5-2 cm の深さまで挿入されます。 3. 胸腔の穿刺 適応症:胸膜炎または水胸症を伴う大量の滲出液による肺の圧迫、および弁性気胸を伴う空気による急激な息切れ。 機器 穿刺は、無菌状態で座位で行われます。 穿刺部位の麻酔には、ノボカインの0,5%溶液が使用されます。 穿刺にはゴム管に接続された太い針を使用します。 肋間血管は下端に沿って配置されているため、肋骨の上端に沿って穿刺が行われます。 胸膜腔への針の貫通は、「ボイドへの失敗」として感じられます。 針に沿った液体の吸引は、針の端が胸膜腔にあることを確認します。 満たされた注射器がゴム管から分離されるたびに、後者は止血クランプでクランプされて、大気が胸膜腔に吸い込まれるのを防ぐ必要があります。 吸引の終わりに、無菌包帯が穿刺部位に適用されます。 合併症:肋間動脈の損傷、肺の横隔膜の血管、胃や腸の穿刺。 気管挿管。 適応症:喉頭の狭窄、病的呼吸、急性呼吸不全、昏睡IIおよびIII度、咽頭、喉頭および気管の疾患における、胸部および腹腔、頭および首の器官への外科的介入中の誤嚥の危険性が高い(急性炎症、がん、結核など)。 挿管には喉頭鏡を使用します。 ハンドルとブレードで構成されています。 より生理学的であるため、最も広く使用されている湾曲したブレード。 ロングネックの直刃を採用。 挿管の準備には、機器のチェックと患者の正しいポジショニングが含まれます。 気管内チューブをチェックする必要があります。 カフは、10 ml 注射器で膨らませてテストします。 喉頭鏡のハンドルと電球とブレードの接触を確認してください。 突然のたんの排出、出血、嘔吐の場合に備えて、吸引の準備ができていることを確認する必要があります。 挿管の成功は、患者の正しい位置に依存します。 患者の頭は、挿管器の剣状突起のレベルにある必要があります。 適度な頭の挙上と環椎後頭関節の同時伸展により、挿管の位置が改善されます。 挿管の準備には、必須の事前酸素化も含まれます。 喉頭鏡は利き手でない方の手 (ほとんどの人は左手) で持ち、もう一方の手で患者の口を大きく開きます。 ブレードは中咽頭の右側に沿って挿入され、歯への損傷を防ぎます。 舌を左にずらし、刃を咽頭弓まで上げます。 湾曲した刃の先端は喉頭蓋谷 (喉頭蓋の前面にある窩) に挿入されますが、まっすぐな刃の先端は喉頭蓋を直接持ち上げる必要があります。 声帯が見えるようになるまで、喉頭鏡のハンドルを下顎に垂直に押し上げます。 歯への依存は避けるべきです。 気管内チューブを右手に取り、視覚制御下で開いた声門を通過させます。 カフは気管上部に配置する必要がありますが、喉頭の下に配置する必要があります。 喉頭鏡は、歯への損傷を避けるために口から取り除かれます。 挿管直後に、両側の肺(一方の気管支にチューブを通すことができるため)と心窩部(食道挿管を除外するため)で聴診を行います。 チューブが気管にある場合は、リボンで位置を固定し、カフを膨らませます。 カフは輪状軟骨のレベルより上に配置する必要があります。これは、喉頭に長く立っていると術後に声がれにつながる可能性があるためです。 合併症:食道の挿管、気管支、喉頭のカフの位置、歯の損傷、下顎の脱臼、喉頭痙攣、反射障害(高血圧、頻脈、頭蓋内圧亢進)、気道の外傷、炎症など 4. 硬膜外腔の穿刺とカテーテル挿入 適応症:重度の疼痛症候群、外科的介入、術後鎮痛の提供。 硬膜外ブロックの設定レベルは、麻酔が必要な臓器によって異なります。 硬膜外穿刺の「対象臓器」の例を表1に示します。 表1 脊柱と「標的臓器」のレベル
器具: 麻酔針、硬膜外腔を穿刺するための特別な針、サンプル注射器、カテーテル、プラグ、フィルター ボール、ナプキン、粘着テープ、滅菌手袋。 患者の位置は、座っているか、横になっています。 この場合、膝とあごをできるだけ胸に近づけます。 したがって、脊椎の最大屈曲が作成され、隣接する椎骨の棘突起間の角度が増加し、黄色の靭帯へのアプローチが容易になります。 無菌条件下で、ノボカインの0,5%溶液による局所麻酔下で、硬膜外腔の穿刺が行われます。 針は厳密に垂直に注入されますが、骨軟骨症では、胸部中央部での穿刺中に傾斜角が生じる可能性があります。 針が靭帯の厚さに入ると、マンドリンがそこから取り除かれ、液体の入った注射器が取り付けられます。 注射器のプランジャーに圧力をかけて、針をさらにゆっくりとスムーズに前進させます。 靭帯の大きな抵抗により、液体は注射器から出ることができません。 注射器を外し、カテーテルを 5 ~ 7 cm 挿入します。抵抗はありません。 針を抜き、ガイドワイヤーを背中に絆創膏で固定し、胸の前面に持ってきます。 フィルター付きプラグは導体に固定されています。 麻酔薬を注射します。 その後、皮膚麻酔のレベルが決定されます。 合併症:呼吸器および血行動態障害、中毒、硬膜の損傷、神経学的合併症、硬膜周囲炎。 5.腰椎穿刺 適応症:髄膜症候群、頭蓋内圧亢進、虚血性脳卒中と出血性脳卒中の鑑別診断、外傷性脳損傷、脊髄腫瘍の存在。 禁忌:穿刺部位での炎症性または化膿性のプロセスの存在、出血性素因、後頭蓋窩の腫瘍、体幹の脱臼、患者の末期状態、視神経の境界がぼやけている。 穿刺点は、腰椎の第 3 棘突起と第 4 棘突起の間にあります。 操作は、局所麻酔下で無菌条件下で行われます。 針はへそに向かって垂直に進みます。 患者の敷設は硬膜外穿刺と同じです。 100本の靭帯(外棘間、内棘間、黄色靭帯)が通過すると、抜け落ち感があり、マンドリンが針から抜け、脳脊髄液が現れます。 検査のために脳脊髄液を採取した後、マンドリンを挿入して針を抜き、無菌ステッカーを貼ります。 硬膜外穿刺とは異なり、硬膜への損傷が発生します。 脳脊髄液は無色透明で、水圧は 200 ~ 0,33 mm です。 アート、タンパク質含有量1003 g / l、HC - 1008-7,35、pH = 7,40-2、糖含有量は血糖の半分に等しい(通常3-110 mmol / l)、塩化物 - 120-5 mmol / l、 XNUMXリンパ球までの細胞数。 合併症:硬膜外炎、大後頭孔への脳の脱臼、神経障害。 第3回 急性意識障害 意識は現実の反映の最高の形であり、人が自分の周りの世界、時間、自分の性格をナビゲートできるようにする一連の精神的プロセスであり、それが自分の行動を保証します。 意識障害は、脳の不可欠な活動の障害の総称であり、環境を適切に知覚、理解、対応し、それをナビゲートし、現在の出来事を記憶し、会話を交わし、恣意的な手段を実行する能力の侵害で表現されます行動行為。 意識の低下(昏迷、昏迷、さまざまな深さの昏睡)、および急性錯乱(せん妄状態または代謝性脳症)にはさまざまな選択肢があります。 意識障害の程度は軽度の錯乱から昏睡までさまざまで、これらの状態の間に明確な移行はありません。 実際には、意識障害の程度は、刺激に対する患者の反応によって決まります。 昏迷は意識障害の一形態であり、無気力、精神的プロセスの進行の鈍化と困難、注意力の急速な消耗、外部刺激の知覚の閾値の増加を特徴としますが、口頭での接触は制限されています。 茫然自失は、注意力の侵害、つまり、必要な情報を選択し、思考と行動の論理的な順序が破られないように応答を調整する能力に基づいています。 昏迷の最も一般的な原因は代謝障害と中毒性障害ですが、皮質の限局性病変、特に右頭頂葉でも観察されることがあります。 そのような患者では、単音節の回答または最も単純な指示の実装を達成することが可能です. 意識がさらに抑圧されると、言語接触の可能性が失われ、痛みが生じます。 Soporは、患者との接触の可能性が失われた意識の深い鬱病の状態ですが、痛み、音、または他の刺激に応答した協調的な防御反応と患者の目の開放は維持されます。 痛みを伴う刺激をしても完全に目覚めることはできず、目を閉じて横になります。 口頭での指示に対する反応は弱いか完全に欠如しており、患者から応答の言葉や音を得るのは不可能です。 意識がさらに圧迫されると、昏睡状態になります。 昏睡状態は、外部刺激に対する無感覚を特徴とする無意識状態です。 これは生命を脅かす中枢神経系の機能の低下と生命機能の調節障害の状態です。 昏睡は、さまざまな代謝障害や構造的損傷によって引き起こされる可能性があります。 昏睡の病態生理 ほとんどの場合、昏睡は次の原因によるものです。 1)脳組織の損傷を伴う頭蓋内プロセス(血腫、膿瘍、腫瘍、てんかん); 2)中枢神経系の感染性病変(髄膜炎、脳炎); 3)脳への毒性損傷(アルコール、キノコ、薬物による中毒); 4) 脳血流の障害 (心静止、Morgani-Adams-Stokes 発作の結果); 5) 代謝の原因 (水分と電解質のバランスの障害、炭水化物の代謝、酸塩基バランス、腎臓と肝臓の機能不全); 6)体温バランスの乱れ(熱中症、低体温症)。 コム分類 病因によると、次の昏睡が区別されます。 1. 原発性、または頭蓋内: 外傷性、血管性、感染性、脳の新生物、てんかん性、代謝性および低酸素性。 2. 二次的、または頭蓋外: 重度の脳損傷。 昏睡の重症度に応じて、次のように分類されます。 1. 患者が痛みを伴う刺激に反応したときの中等度の昏睡。 それらに応じて、屈曲と伸展の動きが現れることがあります。 しかし、保護運動反応は調整されていません。 患者の痛みは目を開けません。 通常、瞳孔反射と角膜反射は維持され、腹部反射は抑制され、腱反射は変化します。 口腔自動症の反射と病的な足の反射の増加。 2. 深い昏睡。 それは、外部刺激に対する反応の欠如、筋緊張のさまざまな変化、両側散瞳を伴わない反射の減少または欠如、自発呼吸および心血管活動の障害によって特徴付けられます。 3. 末期昏睡は、両側性固定散瞳、びまん性筋弛緩、生命機能の重度の違反、調律および呼吸数の障害、無呼吸、重度の頻脈によって決定されます。 血圧が重要であるか、決定されていません。 昏睡患者の診察 患者の検査計画は次のとおりです。 1. 呼吸器系および心血管系の機能状態の評価。 2. 頭蓋外病理を評価することを可能にする、検査データを考慮した一般的な臨床検査。 3.神経学的検査。 臨床検査:一般的な臨床血液検査(細菌またはウイルス感染の徴候); 血液化学: グルコース、凝固因子 (凝固時間、プロトロンビン、フィブリノゲン、APTT、アンチトロンビン III、傍凝固検査、血小板数)、尿素、クレアチニン、ビリルビン、ALT、AST、浸透圧、電解質 (K、Na、Mg、Ca ); 血液、尿、胃内容物の毒物学的スクリーニング。 機器研究: 頭蓋骨と頸椎の X 線撮影。 神経病理学者(神経外科医)の相談により、診断検索のさらなる方向性が決定されます。コンピューターまたは磁気共鳴画像法です。 脳波; 超音波ドップラー検査。 脳脊髄液の分析を伴う腰椎穿刺は、次の後に必須です。 1)眼科医の診察と頭蓋内圧亢進の徴候の除外 - 浮腫および視神経乳頭の上昇; 2) 脳ヘルニアの徴候の排除。 脳ヘルニアの以下の局在が区別されます。 内側テント上局在が損傷したときに発生し、小脳ほぞのノッチを介した間脳の変位からなる間脳ヘルニア。 このプロセスは以下を呼び出します。 1)チェーンストークス呼吸; 2) 光に対する反応を維持しながら瞳孔を収縮させる。 3) 凝視の麻痺; 4) 精神状態の変化。 外側のテント上局在化が影響を受ける場合に発生する側頭葉の内側部分のヘルニアは、小脳テノンのノッチを介した側頭葉の内側部分の変位にある。 結果として生じる中脳の構造への圧力は、次のように表されます。 1) 意識障害; 2) 第 III 脳神経の圧迫に関連する、ヘルニア側の拡大した非反応性の瞳孔。 3) 反対側の片麻痺。 眼球の動きは常に妨げられているわけではありません。 小脳の扁桃腺のヘルニアは、大後頭孔を通して小脳の下部を押す圧力によって引き起こされ、延髄の圧迫につながります。 それは以下を引き起こします: 1)意識障害; 2)呼吸または無呼吸のリズムの違反。 治療 治療は可能な限り積極的に行うべきであり、主に適切な酸素化と中枢血行動態の安定化を確実にすることを目的としています。 自発呼吸が維持されている場合は、マスクまたは鼻カテーテルによる加湿酸素吸入が推奨されます。 自発呼吸がない場合、または病的呼吸がある場合は、気管挿管を行い、患者を人工肺換気に移します。 精神運動の激越と人工呼吸器への反応により、鎮静剤(ベンゾジアゼピン、ブチロフェノン)の使用が必要になります。 中枢血行動態の安定化は、血圧の正常化です。 高血圧状態では、血圧を下げる必要がありますが、10 時間あたり元の血圧の XNUMX% を超えてはなりません。 良い効果は、ニトロプルシドナトリウムまたは硫酸マグネシウムの使用です。 低血圧では、ドーパミン、ドーパミン、ドブトレックス、ホルモン薬が使用されます。 既往歴データがなく、診断が不明確な場合は、ex juvantibus 療法が行われます(薬物曝露に対する肯定的な反応は、一方では診断の鍵を与え、他方では、不可逆的な変化を回避するための時間を得るのに役立ちます): 1)チアミン - 静脈内に100mg、その後 - 筋肉内に100mg(特にアルコール依存症の病歴がある場合、血中の高濃度のエタノールを測定する場合); 2) グルコース - 40 ml の 60% 溶液 (血漿中のグルコース濃度が不明、または 3 mmol / l 未満のレベル)。 3)ナロキソン-0,4-1,2 mgを静脈内に、部分的に、繰り返し、特に「アヘン剤の兆候」(静脈内注射の痕跡、瞳孔の狭さ、中枢性呼吸器疾患)の存在下で。 4) anexat (フルマゼニル) - 0,2 mg を 30 秒間、次の 0,3 分間で、さらに 0,5 mg を次の 3 分間で注入 - XNUMX mg を XNUMX mg の総用量にします。 効果がない場合、昏睡状態がベンゾジアゼピン系薬剤によるものである可能性は低いと考えられます。 5)既知の薬物または物質による中毒または過剰摂取の場合、適切な解毒剤を投与する必要があります(解毒剤療法の可能性がある場合)。 発作制御。脳に低酸素が流入すると、てんかん重積状態を引き起こす可能性があります。発作エピソードは、抗コリンエステラーゼ薬の毒性によって生じることもあります。治療の場合、選択される薬剤はベンゾジアゼピンです。ミダゾラム (Dormikum) 5 mg を分割用量で総用量 30 mg g まで静脈内投与、セデュクセン (Relanium) を分割用量で最大 10 mg まで静脈内投与します。てんかん重積状態が発症すると、ベンゾジアゼピンに続いてフェニトインを総用量1〜1,5 g、速度50 mg/分で投与する必要があります。これらの薬剤に抵抗性がある場合には、フェノバルビタール(チオペンタール)を合計1000mgまでゆっくりと静脈内投与する必要があります(呼吸と血圧の管理が必要です)。発作を繰り返す場合には全身麻酔が必要です。てんかん病巣(出血、新生物、大規模な虚血性梗塞、膿瘍など)のEEGまたはコンピューター断層撮影の兆候がある患者およびエピソード性てんかん発作のある患者では、フェニトインによる維持療法が必要です(経口的に300日XNUMX回XNUMX mg)。 正常体温の維持。直腸温度の制御が必要です。34℃未満の低下は、低体温症、睡眠薬や鎮静剤の過剰摂取、甲状腺機能低下症、ウェルニッケ病によって発症します。このような場合、患者を徐々に36℃まで温める必要があります。低体温症で生命機能が欠如している患者は、低温により心臓と脳の酸素需要が減少し、蘇生処置の結果が向上するため(高カリウム血症を伴う場合を除く)、CPRの対象となります。昏睡状態の患者に発熱がある場合は、感染性合併症の積極的な検索と治療が必要です。髄膜症の兆候の存在は、細菌性髄膜炎またはクモ膜下出血のいずれかの存在を示している可能性があります(ただし、出血の発症から化学的髄膜刺激まで約 12 時間経過する必要があります)。発熱の別の原因は、頭蓋内膿瘍または硬膜下血腫である可能性があります。細菌性髄膜炎が疑われる場合は、頭蓋内圧上昇の兆候を判断するために腰椎穿刺(脳脊髄液分析)およびコンピューター断層撮影を実行する必要があります。 胃内容物の誤嚥を防ぐ。中毒や薬物の過剰摂取の場合には胃洗浄が必要となり、したがって胃チューブの設置により、胃内容物の逆流(胃食道括約筋の弛緩による)のリスクが高まります。したがって、胃チューブを挿入する前に、気道を保護する最善の手段であるシーリングカフを使用して気管挿管を行う必要があります。 泌尿器科治療。利尿を制御するには、フォーリーカテーテルを設置し、無菌状態を確保し、泌尿生殖器敗血症を防ぐための抗菌療法を実施する必要があります。 頭蓋内圧の低下。 ICPの増加は臨床上の緊急事態であり、組織の圧迫や脳血流の減少による脳への二次損傷を回避するために、ICPを低下させるための適切な措置を講じる必要があります。上記の診断手段を実行すると、頭蓋内圧の増加の原因を確立することが可能になり、したがって、主要な手段はその除去を目的としています(手術的および保存的治療)。 pCOレベルを維持するための過換気2 25~30mmHg 美術。 (25 mm Hg 未満のレベルでは、脳血流が大幅に減少し、脳虚血を引き起こす可能性があります)。 水分摂取の制限。 自由水 (5% グルコース) を含む溶液を除外する必要があります。 血液浸透圧を維持するために必要な等張 NaCl 溶液は、半分の用量で投与する必要があります。 浸透圧活性物質の導入。 マンニトールは、1〜2g / kgの用量で10〜20分間投与され、その後、0,05時間ごとに0,3〜6g / kgの維持用量で投与されます。さらに、フロセミドは、ICPをより効果的に低減するために投与されます。 合併症を防ぐには、治療の厳密な管理が必要です。血管内容量の減少、低血圧、高ナトリウム血症、低カルシウム血症、低カリウム血症、および硬膜下血腫の反応症候群と皮質静脈の破裂。 合併症を防ぐための重要な対策は、収縮期血圧を 100 ~ 110 mm Hg に維持することです。 美術。 薬物も ICP の低下につながります。 筋弛緩剤の使用は、機械換気中の ICP を下げるのに役立ちます (機械換気中の胸腔内静脈圧の上昇の遮断)。 コルチコステロイドの使用は、脳の腫瘍形成または限局性虚血(脳卒中)による頭蓋内圧の上昇の場合に有効です。 外傷および一般的な脳虚血による頭蓋内圧亢進の治療におけるコルチコステロイドの有効性は証明されていません。 グルココルチコイドは血糖値の上昇を引き起こし、それに応じて脳虚血を増加させる可能性があることを覚えておくことは重要です. コムの種類 低血糖性昏睡は、真性糖尿病の治療におけるインスリンの過剰摂取または炭水化物摂取の制限によって発生します。 昏睡の発症には、過食症、過敏症、恐怖が先行します。 複視、幻覚、強直性および間代性痙攣が時々認められる。 興奮は無動に置き換えられ、その逆も同様です。 患者はすぐに意識を失い、汗まみれになります。 肌はしっとりと青白く、呼吸は浅くリズミカル。 運動選手や激しい運動の後に、自然発生的な低血糖が観察されることがあります。 低血糖性昏睡が 3 時間以上続くと、中枢神経系に肉眼的な器質的病変が発生する可能性があります。 血糖値を3ミリモル以下に下げることが重要です。 尿中に糖やアセトンはありません。 処理。 すぐにボーラスとして静脈内に 20-40 ml の用量で 20-30% のブドウ糖を入力します。 その後、血糖値と尿糖のコントロールが行われます。 血糖値が急激に上昇した場合の糖尿病性昏睡または高血糖。 昏睡の前には、眠気、喉の渇き、食欲不振、吐き気、嘔吐、頭痛があります。 高血糖、代謝性アシドーシスは実験室で測定され、尿中に糖とアセトンが存在します(常にではありません)。 顔は青白く充血しており、粘膜は乾燥しており、皮膚も乾燥しており、膨満感が低下しています。 眼球がくぼんでいて、口からアセトンの匂いがする可能性があります。 呼吸はまれな病的です。 血行動態が乱れています:頻脈、動脈性低血圧、こもった心音。 処理。 3日あたり5〜6リットルの量の塩化ナトリウムの静脈内投与の助けを借りて血液量減少の除去。 インスリン療法は、輸液ポンプを使用して10時間あたり11〜13IUの短時間作用型インスリンを導入することで構成されます。 血糖値が4〜8 mmol / lに低下すると、インスリンの投与量は5時間あたりXNUMX〜XNUMX単位に減少し、XNUMX%ブドウ糖の注入により低血糖状態が回避され始めます。 甲状腺中毒性昏睡はまれですが、重度の頻脈があり、血行動態心筋不全の典型的な徴候がなく、エネルギー動態性心不全がある場合は、考慮する必要があります。 通常、ストマ、目のまぶしさ、振戦の存在も、この可能性に注意を向けます。 診断を確認する研究(基礎代謝、放射性ヨウ素)を実施できないため、既往歴データを収集して臨床像を補足する必要があります。 アルコール中毒は、口からのアルコール臭、錯乱状態、不安、嘔吐、顔のむくみなどによって現れます。 呼吸が遅くなり、脈拍が速くなり、瞳孔が拡張します。 アルコール依存症の患者では、アルコール離脱後 2 ~ 3 日でせん妄が発症します。 せん妄の発症は、危険信号(発熱、振戦、頻脈、高血圧)が現れたときにベンゾジアゼピンを使用することで予防されます。 せん妄の発症に伴い、選択される薬は次のとおりです。若い人ではジアゼパム(静脈内投与)、高齢者や肝機能障害のある患者ではロラゼパムですが、必要に応じて、ジアゼパムよりも迅速な効果が望ましいです(5mgごとに効果が得られるまで5分)。 重度のせん妄状態の治療のために 2640 mg のジアゼパムを投与する必要がある場合が記載されています。 さらに、ブロッカーとクロニジンが使用されます。 また、これらの状態では、抗精神病薬(ハロペリドール、ドロペリドール)の使用が役立ちます。 脳卒中昏睡(さまざまな脳内プロセスで発症)の主な症状は、片麻痺または個々の筋肉群の麻痺です。 目と頭が麻痺者とは反対の方向に向けられると、麻痺が現れます。「患者は脳の病変を見ます」。 口は健康側に偏っている:「病気の側でパイプを吸っている」。 片麻痺側では、持ち上げられた手足がベッドに素早く重く落ちますが、影響を受けていない手足はゆっくりと元の位置に戻ります。 アジソン病による昏睡(副腎性昏睡、副腎結核、外傷、感染症で発症することが多い)はまれです。 主な症状は病理学的に低く、しばしば測定不能な血圧です。 虚脱とともに、この症状は炭水化物代謝の変化(低血糖)、電解質の不均衡および水分代謝によって引き起こされます。 突然、鋭い蒼白、冷や汗が出る。 興奮はすぐに無力症に変わり、患者は意識を失います。 先端チアノーゼが現れ、皮膚が大理石になります。 背中と四肢の皮膚に、色素沈着が黒い斑点と真っ赤な点状の発疹の形で見られます。 心音がこもっている。 脱水症状と乏尿がすぐに始まります。 血中、代謝性アシドーシス、低血糖、および残留窒素の増加。 治療は、1mg/kgの用量で糖質コルチコイドを迅速に導入することからなる。 投与量は2〜3倍に増やすことができます。 同様の用量が筋肉内に投与されます。 脱水症と戦うために、塩化ナトリウムの等張液が投与され、次にブドウ糖が投与されます。 講義番号4.心肺蘇生法 心肺蘇生法 (CPR) は、生命を脅かす怪我がない場合に実行される外科的および治療的措置の複合体であり、心肺系の機能の回復とサポートを目的としています。 心肺蘇生の適応症:頸動脈に有効な脈拍がない、または脈が弱く弱い、意識がない、および(または)効果的な呼吸運動がない患者で実施されます。 一次心停止および一次呼吸不全の最も一般的なケース。 禁忌:生命と相容れないトラウマ、不治の病の末期、生物学的死。 基本原則 CPRの主な取り組みは、次のことを目的としています。 1)胸部圧迫; 2) 肺と換気に空気を吹き込みます。 3) 薬剤の調製および投与; 4)静脈内アクセスの設置と維持。 5) 専門的な活動 (除細動、ペースメーカーの設置、気管挿管)。 したがって、活動の全範囲を完了するには、4 人とチームリーダーが必要です。 40 人が CPR を担当する必要があります。 この担当者は、利用可能なすべての情報を統合し、影響を優先する必要があります。 彼は心電図モニター、薬物の使用を監視し、他のチームメンバーの行動が修正されていることを確認する必要があります. 彼は、リーダーシップの役割を損なう手順の実行から除外されるべきです. XNUMX 年以上にわたり、Safar 蘇生アルファベットは CPR に使用されてきました。 この複合体では、蘇生器の一連の動作が維持されます; 英語名によると、それらは対応する文字で示されます。 A - 気道 - 気道の開通性を確保します。 B - 呼吸 - アクセス可能な方法での肺の人工換気 (ALV)。たとえば、「口から口へ」呼吸する場合。 C-循環-血液循環の確保-間接心臓マッサージ。 D-薬物-薬物の導入。 E - 心電図検査 - ECG 登録。 F - 細動 - 必要に応じて、電気的除細動 (カーディオバージョン) を行います。 G - 測定 - 一次結果の評価。 H - 低体温 - 頭部冷却。 I-集中治療-蘇生後症候群の集中治療。 A - 気道 - 気道管理 患者は仰向けに水平に置かれます。 頭は可能な限り後ろに倒されます。これは、医師が片手を首の下に置き、もう一方の手を患者の額に置くためです。 テスト呼吸は口から口へと行われます。 筋緊張が低下した患者が仰向けになると、喉を詰まらせるように舌が沈むことがあります。 同時に、喉頭蓋が下降し、気道をさらに塞ぎます。 出現:呼吸が響き、呼吸リズムが完全に停止するまで違反します。 このような現象は、無意識の患者で特に急速に発症します。 舌の後退を防止および解消するには、下顎を前に出すと同時に、後頭頸部関節の過伸展を行う必要があります。 これを行うには、親指をあごに押し付けて、患者の下顎を下に動かし、指を顎の角に置いて前方に押し、頭を後方に過度に伸ばすことでこの技術を補完します(トリプルサファーテクニック)。 これらの操作を正しくタイムリーに行うことで、咽頭レベルでの気道の開存性が迅速に回復します。 異物(血栓、粘液、入れ歯など)が気道閉塞の原因になることがあります。 それらは即席の材料(ナプキン、ハンカチ)ですぐに取り除かれます。 誤嚥の危険があるため、患者の頭を横に向ける必要があります。 上気道の開存性の回復は、さまざまなエアダクトの使用によって促進されます。 S字ダクトの使用が最適です。 その導入のために、患者の口は交差した指 II と I で開かれ、口蓋に沿って開口部が「スライド」するように、チューブが舌の付け根まで進められます。 輸送中にエアダクトが動かないように注意する必要があります。 記載されているすべての手順が効果的でない場合は、下にあるセクションに気道の閉塞が存在すると想定できます。 これらの場合、直接喉頭鏡検査と病理学的分泌物の積極的な吸引が必要であり、続いて 10 ~ 15 秒間の気管挿管が必要です。 円錐切除術と気管切開術を行うことをお勧めします。 B-呼吸-アクセス可能な方法での人工肺換気(ALV) 蘇生中の人工呼吸の最も簡単で最も効果的な方法は、蘇生者の呼気が圧力下で犠牲者の肺に吹き込まれる「口対口」法です。 犠牲者の頭を投げ返した後、片方の手で鼻孔をつまみ、もう一方の手を首の下に置き、深呼吸をして、犠牲者の唇(子供では唇と同時に鼻をかむ)そして犠牲者の肺に空気を吹き込み、吸入時間中の胸の上昇を観察します。 胸が上がるとすぐに空気の注入が止まり、顔を横に動かし、再び深呼吸をします。このとき、患者は受動的な呼気をします。 肺を2〜3回膨張させた後、頸動脈の脈拍の存在が判断され、検出されない場合は、血液循環の人為的な回復に進みます。 手動換気は、自動拡張式の Ambu タイプのバッグを使用して使用されます。 人工呼吸器を使用する場合、呼吸数は毎分 12 ~ 15 回、吸気量は 0,5 ~ 1,0 リットルです。 病院では、気管挿管が行われ、患者は人工呼吸器に移されます。 C-Circulation - 血液循環の確保 - 間接心臓マッサージ 閉鎖心臓マッサージは、緊急人工循環支援の最も簡単で効率的な方法です。 閉鎖心臓マッサージは、その原因とメカニズムを明らかにすることなく、急性循環停止の診断が下されたらすぐに開始する必要があります。 効果のない心臓収縮の場合、完全な心停止または適切な心臓活動の独立した回復を待つべきではありません。 閉心マッサージの基本ルール。 1. 患者は、マッサージの手の強さの下で彼の体の変位の可能性を防ぐために、しっかりしたベース (床または低いソファ) の上に水平な位置にいる必要があります。 2.蘇生器の手の力の適用ゾーンは、厳密に正中線に沿って、胸骨の下XNUMX分のXNUMXにあります。 蘇生器は患者のどちらの側にも配置できます。 3.マッサージのために、一方の手のひらをもう一方の上に置き、剣状突起の胸骨への付着場所より3〜4本の横指に位置する領域の胸骨に圧力をかけます。 肘の関節でまっすぐにされたマッサージャーの手は、手首だけが圧力をかけるように配置されます。 4.犠牲者の胸部の圧迫は、医師の胴体の重力によって行われます。 胸骨の脊椎への変位(つまり、胸部のたわみの深さ)は4〜6cmである必要があります。 5. 0,5 回の胸部圧迫の持続時間は 0,5 秒で、個々の圧迫の間隔は 1 ~ 60 秒です。 マッサージの速度 - XNUMX分間にXNUMX回のマッサージ動作。 間隔を置いて、手は胸骨から取り外されず、指は上げられたままになり、腕は肘関節で完全に伸びます。 15 人で蘇生を行う場合、患者の肺に空気を 2 回すばやく注入した後、15 回の胸骨圧迫が行われます。つまり、「換気:マッサージ」の比率は 2:1 です。この比率は 5:5 です。つまり、XNUMX 回の呼吸で胸骨圧迫が XNUMX 回行われます。 心臓マッサージの前提条件は、その効果を常に監視することです。 マッサージの有効性の基準は、次のように考慮する必要があります。 1. 皮膚の色の変化: 薄くなり、灰色になり、チアノーゼになります。 2.瞳孔が拡張した場合、光に対する反応の出現を伴う瞳孔の収縮。 3.頸動脈と大腿動脈、時には橈骨動脈にパルスインパルスが現れる。 4. 60〜70 mm Hgのレベルでの血圧の測定。 美術。 肩で測ったところ。 5.時には独立した呼吸運動の出現。 血液循環の回復の兆候があるが、独立した心臓活動を維持する傾向がない場合は、望ましい効果が得られるまで(有効な血流の回復)、または生命の兆候が永久に消えるまで、心臓マッサージが行われます脳死の症状の発症に伴い。 25〜30分間の心臓マッサージにもかかわらず、血流の減少さえも回復の兆候がない場合、患者は死にかけていると認識されるべきであり、蘇生措置を中止することができます. D - 薬物 - 薬物投与 血液循環が急激に停止した場合は、心臓の活動を刺激する薬剤の導入をできるだけ早く開始し、必要に応じて蘇生中に繰り返す必要があります。 心臓マッサージの開始後、アドレナリン 0,5 ~ 1 ml をできるだけ早く (静脈内または気管内に) 投与する必要があります。 2~5分で繰り返し導入可能(合計5~6mlまで)。 心静止では、アドレナリンは心筋の調子を整え、心臓の「開始」を助けます。心室細動では、小波細動から大波への移行に寄与し、除細動を大幅に促進します。 アドレナリンは冠状動脈の血流を促進し、心筋の収縮性を高めます。 エピネフリンの代わりに、心筋への効果の点でアドレナリンよりも3倍効果的なイソドリンを使用できます。 最初の投与量は 1 ~ 2 ml を静脈内投与し、次の投与量は 1 ml の 2% グルコース溶液で 250 ~ 5 ml です。 血液循環障害の状態では、代謝性アシドーシスが徐々に増加するため、アドレナリンの注入直後に、重炭酸ナトリウムの4〜5%溶液を患者の体重3 kgあたり0,1 mlの速度で静脈内投与します。 死の過程で、副交感神経系の緊張が大幅に高まり、脳が枯渇するため、M-コリン溶解薬が使用されます。 心静止および徐脈では、アトロピンは0,5%溶液(1〜3 ml、最大用量4〜5 ml)で静脈内投与されます。 心筋緊張を高め、高カリウム血症の影響を軽減するために、塩化カルシウムの10%溶液XNUMXmlの静脈内投与が推奨されます。 アドレナリン、アトロピン、塩化カルシウムを同じ注射器で一緒に投与できます。 重度の頻脈、特に細動の発症では、リドカインを60〜80 mgの用量で使用することが示されていますが、短時間作用型であるため、2mg/分の速度で注入されます。 カテコールアミンに対する副腎反応性心筋構造の感受性を高め、細胞膜の透過性を正常化することにより、適切な心臓活動の回復に寄与する糖質コルチコイドを使用することも示されている。 E-心電図-ECG登録 ECG研究の助けを借りて、心臓活動の違反の性質が決定されます。 ほとんどの場合、それは心静止 - 心臓収縮の完全な停止、細動 - 心拍出量が実質的に停止する400〜500拍/分の頻度での心筋線維の無秩序な非協調収縮である可能性があります。 最初に、大波細動が認められ、1〜2分以内に小波細動に移行し、その後心静止が続きます。 心電図にリズムが存在することは、心筋の電気的活動が完全に存在しないことよりも優れています。 したがって、CPR の重要なタスクは、心筋の電気的活動を刺激し、その後、効果的な (脈拍の存在) リズムに変更することです。 心静止の存在は、重度の心筋灌流障害のマーカーとして機能し、心臓のリズムを回復するための予後不良の兆候として機能します。 ただし、低振幅マイクロ波心室細動と心静止を区別することが重要であり、これは標準的な ECG リード 2 ~ 3 で行うのが最適です。 アドレナリン (1 mg の静脈内投与) とアトロピン (1 mg を 2 ~ 4 mg に増量) は、電気的活動の回復に最も効果的です。 難治性の場合、カリウムとカルシウムのレベルの補正が有効です。 心室細動 (VF) VF は突然死の最も一般的な原因であり、除細動の成功は除細動の実施時期によって大きく左右されるため、脈拍のない患者では、(循環停止の原因が ECG によって認識される前に) 直ちにブラインド電気インパルス療法を実施する必要があります。 . 「ブラインド」除細動は心静止や徐脈の患者に害を及ぼさず、通常は頻脈や VF の患者に有効であることに注意してください。 子供は VF よりも末期疾患の原因として呼吸停止を起こす可能性がはるかに高いため、「盲目的な」電気的除細動のルールは子供には受け入れられないことを覚えておくことが重要です。 除細動の成功は、VF の振幅に左右されます。VF の振幅は、VF エピソードの持続時間と逆相関しています。 カルディオバージョンの最初の XNUMX 回の試みが効果がない場合、アドレナリンを投与して、細動波の振幅を増加させ、血管緊張を高める必要があります (心拍リズムが回復した場合は、心臓と脳の灌流を増加させることができます)。 一方、心筋の酸素需要を増加させないように、最適な用量のアドレナリンを使用する必要があります。 F - 細動 - 必要に応じて電気除細動を行います(カーディオバージョン) 心細動は、電気除細動器を使用することで解消できます。 電極を胸にしっかりと適用する必要があります(前外側位置では、XNUMXつの電極が心臓の頂点の領域にあり、XNUMX番目の電極が胸骨の右側の鎖骨下領域にあります)。放電、したがって除細動の有効性。 多くの患者では、電極の前後 (心臓の頂点 - 肩甲骨間) の位置がより効果的です。 ECG モニターのオーバーレイの上に電極を適用しないでください。 電気的除細動は、心電図上で 0,5 ~ 1 mV 以上の振幅の大波動が記録された場合にのみ有効であることに注意してください。 この種の心筋細動は、そのエネルギー資源の安全性と、適切な心臓活動を回復する可能性を示しています。 重度の心筋低酸素症で観察される振動が低く、不整脈的で多形性である場合、除細動後の心臓活動の回復の可能性は最小限です。 この場合、心臓マッサージ、人工呼吸器、アドレナリン、アトロピン、塩化カルシウムの静脈内投与の助けを借りて、細動から大波への移行を達成する必要があり、その後除細動を行う必要があります。 除細動の最初の試行は200 Jの放電で実行され、その後の試行で電荷は360 Jに増加します。電極を湿らせ、胸の表面にしっかりと押し付ける必要があります。 除細動の無効化の原因となる除細動中の最も一般的なエラーには、次のようなものがあります。 1.除細動器の退院準備中、心臓マッサージの長時間の中断または蘇生法の完全な欠如。 2.電極の緩い押し付けまたは不十分な湿潤。 3.心筋のエネルギー資源を増加させる対策を講じることなく、低波細動を背景に放電を適用します。 4.低電圧または過度に高電圧の放電を適用します。 心臓の電気的除細動は、発作性心室頻拍、心房粗動、結節性および上室性頻脈、心房細動などの心不整脈を修正するための効果的な方法であることに注意してください。 入院前段階での電気的除細動の適応は、ほとんどの場合、発作性心室頻拍です。 これらの状態での除細動の特徴は、患者の意識の存在と、放電を適用する際の痛みへの反応を排除する必要があることです。 G - ゲージング - 一次結果の評価 結果の一次評価は、循環器系および呼吸器系の状態を確認するためだけでなく、さらなる治療手段の戦術を概説するためにも行われます。 心臓活動の回復が見られる蘇生プロセスが完了すると、蘇生者はいくつかの最終アクションを実行する必要があります。 1)気道の状態を評価する(呼吸の対称性、強制呼吸の継続、換気の妥当性); 2)中枢および末梢動脈の脈動をチェックします。 3)肌の色を評価します。 4)血圧のレベルを決定します。 5) 循環血液量を測定する (CVP を測定し、頸静脈の状態を評価する)。 6) 中心静脈のカテーテルの正しい位置を確認します。 7)突然死の原因となった心房細動が解消された場合は、心房細動剤の注入を継続してください。 8) 突然死のエピソードの前に患者に行われた場合、治療を修正する。 H - 低体温症 - 頭の冷却 低体温症では、循環停止の臨界時間が大幅に増加する可能性があります。 低酸素後脳症の発症を防ぐために、脳内の代謝プロセスの強度を低下させるための対策、および抗低酸素薬および抗酸化薬を使用する必要があります。 主な活動 1.頭蓋脳低体温 - 頭と首をアイスパック、雪、冷水で包みます。 2.抗低酸素剤(オキシ酪酸ナトリウム、マフソール、少量の鎮静剤)の非経口投与、および血液のレオロジー特性の改善(レオポリグルシン、ヘモデス、ヘパリン、トレンタール)。 3. カルシウム拮抗薬(ニモトン、リドフラジンなど)の導入。 4.抗酸化物質(マフソル、ユニティオール、ビタミンC、カタラーゼなど)の導入。 I - 集中治療 - 蘇生後症候群の集中治療を実施する CPR に対する迅速な陽性反応は、患者の予後が良好である可能性を高めますが、その後、敗血症、急性肺不全、および肺炎を発症する可能性があり、自然に予後を悪化させます。 この期間中に病変が深まり、自律制御と防御反射の維持を提供する神経中枢が損傷するため、CPR後の重要臓器の以前の疾患を有する患者の長期生存は典型的ではありません。 また、集中的な胸骨圧迫を使用すると、肝臓の破裂、大動脈、気胸、肋骨および胸骨の骨折が認められます。 誤嚥性肺炎、痙攣(脳虚血による)、リドカイン中毒が一般的な合併症です。 多くの患者は、胃と十二指腸のストレス性潰瘍から出血します。 CPR 後、肝臓 (および/または骨格筋) の酵素レベルが大幅に上昇しますが、肝臓壊死の発生およびその機能不全はまれです。 高エネルギー除細動レジメンでは、クレアチンホスホキナーゼのレベルが大幅に増加しますが、MB 画分の増加は、高エネルギー放電が繰り返された場合にのみ存在します。 1.CBSと水電解質バランスの修正。 多くの場合、心肺蘇生の後、代謝性アルカローシス、低カリウム血症、低塩素血症、その他の電解質障害が発生します。 酸性環境またはアルカリ性環境への pH のシフトがあります。 pH 補正の鍵は十分な換気です。 重炭酸塩の使用は、血液のガス組成の制御下で実行する必要があります。 原則としてNSOの導入は不要3 血液循環と呼吸が急速に回復します。 心臓が機能している場合、心血管系の機能には 7,15 以下の pH レベルが適切です。 一般的に推奨される重炭酸塩の用量 (1 mg/kg) は、次のような副作用を引き起こす可能性があります。 1) 不整脈性アルカローシス; 2) CO生産の増加2; 3) 高浸透圧; 4) 低カリウム血症; 5) 中枢神経系の逆説的な細胞内アシドーシス; 6) Oの組織供給を制限する、ヘモグロビン解離曲線の左へのシフト2. したがって、この薬の任命は厳密に適応症に従う必要があります。 低カリウム血症を解消するために、塩化カリウムの静脈内注入が2日あたりXNUMXミリモル/kgの用量で実行されます。 2. 抗酸化防御システムの正常化。 集中治療には、マフソール、ユニチオール、ビタミンC、マルチビオント、トコフェロール、プロブコールなど、多方向作用を持つ抗酸化薬の複合体が含まれます。 3. 抗酸化物質の使用は、代謝プロセスの強度を低下させるのに役立ち、その結果、酸素とエネルギーの必要性を低下させ、低酸素時に利用できる酸素の減少量を最大限に活用します。 これは、神経栄養保護薬と抗低酸素薬(セジュセン、ドロペリドール、ガングリオンブロッカー、メキサミン、ヒドロキシ酪酸ナトリウム、シトクロム、グチミンなど)の使用によって達成されます. 4.エネルギー資源の増加は、インスリンとエネルギー利用に関与する主要な補酵素(ビタミンB)を含む濃縮グルコース溶液の静脈内投与によって提供されます。6、コカルボキシラーゼ、ATP、リボキシンなど)。 5.タンパク質と核酸の合成の刺激 - 細胞の正常な機能、酵素、免疫グロブリンなどの合成に絶対に必要な基質は、同化ホルモン(レタボリル、ネラボリル、インスリン、レチノール)の使用によって行われます)、葉酸、およびアミノ酸溶液の導入。 6.好気性代謝の活性化は、十分な量の酸化基質(グルコース)を導入し、双曲線酸素化(HBO)を使用することによって達成されます-この方法は、その送達の急激な違反の条件でも必要な量の酸素の供給を保証します。 7. 酸化還元プロセスの改善 (コハク酸、リボキシン、トコフェロールなど)。 8.積極的な解毒療法は、代謝プロセスの正常化に貢献します。 そのために、さまざまな輸液療法(ゼラチノール、アルブミン、血漿)や強制利尿などの方法が用いられ、重症例では体外解毒法(血液吸着、血液透析、血漿交換)が用いられます。 9.微小循環プロセスの違反の排除。 このために、ヘパリン療法が行われます。 すべての臨床状況に対応する単一のガイドラインはありません。 進行中の CPR の間、神経学的徴候は転帰のマーカーとして機能できず、したがって、CPR が停止されたときに神経学的徴候によって導かれることはありません。 調整された心拍リズムを回復するのに 20 分以上かかる場合、蘇生はほとんど効果がありません。 いくつかの研究は、完全な CPR に対して 30 分以内に応答がないと、まれな例外を除いて、死に至ることを示しています。 最良の結果は、即時の効果的な除細動の場合に発生します。 低体温症および中枢神経系の深い薬理学的抑制(バルビツレートなど)により、良好な神経学的転帰を伴う長期の蘇生が可能です。 脳の生存不能性を判断する方法: 1)脳血管の血管造影(血流の欠如); 2) EEG (少なくとも 24 時間の直線); 3) コンピュータ断層撮影。 CPR終了基準: 1) 30 分以内に蘇生処置を正しく行っても効果がない場合 - 自発呼吸が現れず、血液循環が回復せず、瞳孔が散大したままで光に反応しません。 2)30分以内に、治療に適さない心停止が繰り返され、同時に蘇生が成功した他の兆候がない場合。 3) 蘇生の過程で、この患者がまったく表示されていないことが判明した場合。 4) 45 ~ 60 分以内に、呼吸が部分的に回復したにもかかわらず、被害者に脈拍がなく、脳機能の回復の兆候がない場合。 講義 No. 5. 呼吸器科における緊急事態 急性呼吸不全は、外部呼吸装置の機能が体に酸素を供給し、二酸化炭素を適切に除去するのに不十分である体の病理学的状態です。 通常の一回換気量 (TO) は 500 ml (肺胞換気 - 350 ml、死腔 150 ml) です。 分時換気量 (MOV) - 6-8 l。 酸素消費量 - 300 ml/分。 呼気中の酸素は16%、吸入中 - 21%です。 吸入混合物中の酸素は少なくとも 20% でなければなりません。 急性呼吸不全の原因:肺の最終的な構造的および機能的単位であるレスピロンのレベルでの呼吸の中央調節の違反または換気と血流の不一致。 麻薬物質の過剰摂取(吸入)、麻薬性鎮痛薬、急性脳浮腫、脳血管障害、脳腫瘍、気道内腔の減少または完全閉塞、舌の退縮、大量の喀痰、特に化膿性肺疾患(膿瘍、両側性)の患者気管支拡張症)、肺出血、嘔吐および誤嚥、喉頭痙攣および気管支痙攣。 舌が引っ込められたら、空気ダクトを配置するか、挿管して人工呼吸するのが最も確実です。 喀痰の蓄積により、患者に喀痰を強制する必要があります。 患者が意識を失っている場合、気道は消毒されます。 重度の患者では、麻酔と積極的な衛生管理が行われます。 気管、気管支樹のカテーテル挿入と内容物の除去が行われます。 1.喉頭痙攣 喉頭痙攣は、真声帯と偽声帯の閉鎖です。 どちらの場合も、制御剤(ユーフィリン)が必ず使用されます。 これで問題が解決しない場合は、短時間作用型の筋弛緩剤を導入し、挿管して患者を人工呼吸器に移す必要があります。 筋弛緩剤は、十分な脱キュラリゼーションが行われないと、術後に呼吸不全を引き起こします。 通常、抗コリンエステラーゼ薬(プロゼリン)によって産生されます。 抜管の時までに、筋力と筋緊張が回復していることを確認する必要があります(手を上げ、手を絞って、頭を上げるように依頼してください)。 肋骨の複数の骨折により、吸入時に胸の一部が沈み、いわゆる逆説呼吸が発生するため、胸のフレームを復元する必要があります。 この患者の場合、弛緩剤を導入した後、挿管し、人工呼吸器にさらに移行する必要があります (胸部の完全性が回復するまで)。 以下は、機能している肺実質の減少につながります:無気肺、肺虚脱、肺炎、手術の結果、肺炎、出血、膿胸。 無気肺と虚脱の違い:無気肺はまっすぐな状態の障害物です。 この状態は、循環血液の半分が通過する換気されていない肺の存在によって特徴付けられます。後者は酸素化されていません。 その結果、急性呼吸不全が発症します。 肺がつぶれると、胸腔内の空気または液体によって圧縮されます。 同時に、圧縮された肺の血液循環は急激に減少し、健康な肺の血液循環は増加します。 したがって、虚脱は、急性呼吸不全の発症という点で、無気肺ほど危険な合併症ではありません。 手術前に、無傷の肺の機能を評価する必要があります (別のスピログラフィー)。 発達段階に応じて、急性呼吸不全は次のように分類されます。 1)機能障害; 2) 不足; 3) 補綴機能の障害。 発症率に応じて、急性呼吸不全は次のように分類されます。 1)電光石火の速さ(XNUMX分以内に発症); 2) 急性 (数時間以内に発症); 3) 亜急性 (数日以内に発症); 4)慢性(何年も続く)。 急性呼吸不全の集中治療の主な要素:酸素療法、患者の排液位置、線維気管支鏡検査、気管切開、挿管および人工呼吸、気管支拡張、ホルモン療法、HBO。 2. 肺塞栓症 肺塞栓症(PE)は、肺動脈の主幹または中幹、小さな血管幹の閉塞であり、肺循環の圧力の上昇、右心室不全を引き起こします。 素因 心血管系の疾患-アテローム性動脈硬化症、リウマチ性心臓病、リウマチ性奇形、敗血症性心内膜炎。 下肢の静脈の病気、小骨盤の臓器や血管の病理。 特に術後PEには細心の注意が必要です。 ほとんどの場合、塞栓症は、下肢の血管、膀胱、女性の生殖器、前立腺、骨盤、股関節の手術中に発症します。 止血、自発的な線維素溶解、静脈血栓の収縮および組織化のシステムの変化は不可欠です。 さまざまな理由でベッドにとどまることを余儀なくされている腫瘍性疾患、肥満、循環不全の患者も最大のリスクにさらされています。 PEの臨床分類 フォーム:ヘビー、ミディアム、ライト。 下流:劇症、急性、再発。 肺動脈への損傷のレベルによると:幹または主枝、葉(分節)枝、小枝。 クリニックと診断 PE の臨床経過は非常に多様です。 最も一般的な症状は、突然の息切れ (RR の範囲は 30 分あたり 50 から XNUMX 以上)、急速な呼吸、蒼白、しばしばチアノーゼ、頸静脈の腫れ、頻脈、動脈性低血圧 (ショックまで)、胸骨後部です。痛み、咳、喀血。 聴診は、しばしば肺動脈上の II トーンの強化を決定します。 X線の兆候-近位肺動脈のサイズの増加、末梢パターンの枯渇、および横隔膜のドームの上昇。 心電図は、適切な部門(肺性心)の過負荷を明らかにする場合があります。 1)R波とS波の振幅が同時に増加するQ波の出現(QS症候群); 2)右心室を前方にして縦軸を中心に心臓を回転させる(左胸への移行帯のシフト)。 3) 誘導 III、aVF、V1-V3 における負の T 波を伴う ST セグメントの上昇; 4)ヒス束の右脚の封鎖の出現または程度の増加。 5)電気軸が右にずれている、尖った「肺」歯P。 6)洞性頻脈または心房細動の頻脈性形態。 心エコー検査により、急性肺性心の検出、肺循環における高血圧の重症度の決定、右心室の構造的および機能的状態の評価、心腔および主肺動脈における血栓塞栓症の検出、卵円孔の開放の可視化が可能になります。血行動態障害の重症度と逆説的塞栓症の原因となります。 しかし、心エコー検査の結果が陰性であっても、肺塞栓症の診断が否定されるわけではありません。 最も有益な診断方法は、肺動脈造影です。 予防目的で、抗凝固剤が術後に使用されます。 ヘパリンの投与量は 10 日 000 IU(2 IU を 500 回)です。 禁忌がある場合、抗凝固薬は処方されません。 禁忌は次のとおりです。重度の脳損傷。 出血の可能性がある腫瘍病理; 血小板減少症; 肺結核; 機能不全を伴う肝臓および腎臓の実質の重度の慢性疾患。 治療 抗凝固療法。 抗凝固薬は、肺血管床の二次血栓症と静脈血栓症の進行を防ぐことができます。 従来の未分画ヘパリンと比較して、出血性合併症を起こしにくく、血小板機能への影響が少なく、作用持続時間が長く、バイオアベイラビリティが高い低分子量ヘパリン(ダルテパリン、エイオキサパリン、フラキシパリン)を広く使用することをお勧めします。 血栓溶解療法。 大規模なPEでは、病変の体積が比較的小さいが、肺高血圧症が顕著である場合に、血栓溶解療法が示され、正当化されます。 ほとんどの場合、ストレプトキナーゼは 100 時間あたり 000 単位の用量で使用されますが、重度のアレルギー反応に注意する必要があります。 血栓溶解の期間は通常 1 ~ 2 日です。 ウロキナーゼとアルテプラーゼには抗原性がありませんが、高い耐性があります。 手術。 塞栓摘出術は、顕著な血行動態障害を伴う、極めて重度の肺灌流障害を伴う肺幹またはその両方の主枝の血栓塞栓症の患者に適応となります。 大静脈のクロスクランプ後に塞栓を除去するためのすべての操作は、3 分以内に行う必要があります。この間隔は、初期の重度の低酸素状態で手術を受ける患者にとって重要だからです。 経胸骨アクセスを使用して心肺バイパス下で塞栓摘出術を行うのが最適です。 3.気管支喘息 気管支喘息は、自己免疫成分を伴う気道の慢性炎症に基づく疾患であり、気管支の感受性と反応性の変化を伴い、発作または窒息の状態によって現れ、呼吸器の不快感の症状が絶えず発生します。アレルギー性疾患の遺伝的素因の。 分類 気管支喘息の分類は以下の通りです。 1.喘息の発症段階: 1) 実質的に健康な人の生物学的欠陥; 2)preastmaの状態; 3)臨床的に顕著な喘息。 2. 臨床的および病的バリアント: 1) アトピー; 2) 感染依存性。 3) 自己免疫; 4) 不調和; 5) 神経精神的; 6)吸引; 7)一次変化した気管支反応性。 3.病気の経過の重症度: 1)肺; 2) 中等度; 3) 重い。 4. フロー フェーズ: 1) 悪化; 2)不安定な寛解; 3) 安定した寛解 (2 年以上)。 5.合併症: 1)肺-無気肺、気胸、急性肺動脈弁閉鎖不全症; 2) 肺外 - 肺性心、心不全。 6.病因別: 1)アトピー(外因性、アレルギー性、免疫性); 2)非アトピー(内因性、非免疫学的)。 BA の程度の臨床基準を表 2 に示します。 表2 喘息の重症度を評価するための臨床基準
喘息状態 喘息の状態は、日中の急性閉塞性呼吸不全を特徴とする気管支喘息の止まらない発作です。 喘息状態の主な際立った特徴は、従来の気管支拡張薬療法の効果の欠如と非生産的な衰弱性の咳です。 喘息重積状態の分類を表3に示します。 表3 喘息状態の分類 (Sorokina T. A., 1987)
ASは、呼気性の重度の息切れを特徴とし、胸部の補助筋肉と前腹壁が呼吸行為に関与し、皮膚の色の変化(蒼白、充血、チアノーゼ)を伴います。 皮膚は乾燥して熱くなったり、冷たくて湿ったりすることがあります。 頻呼吸が特徴的で、呼吸数は通常 30 分間に 1 回以上です。 狭くなった細気管支を通る空気の通過に関連する音楽の音を聴診で聞く。 プロセスの進行に伴い、肺の「サイレントゾーン」というよく知られた現象が発生します。これは、肺のこの領域の気管支閉塞を示しています。 頻脈、血圧の上昇、心拍出量(MOS)が特徴です。 吸気中の収縮期血圧の低下。 脱水症と血液量減少が発生します。 水分の喪失は主に気道と皮膚を通して起こります。 循環血液(CBV)の量は通常、平均10%減少し、増加することはめったにありません。 血液の粘度とヘマトクリット値を0,50〜0,60に大幅に増加させます。これにより、肺血栓塞栓症の本当の脅威が生じ、ヘパリンの指定が必要になります。 タンパク質の濃度が増加し、一般的な脱水症は、喉の渇き、舌の乾燥、血漿浸透圧の増加、および乏尿によって現れます。 中心静脈圧(CVP)は2〜5cmの水に低下します。 美術。 循環血液量減少は崩壊しやすくなります。これは、患者を人工呼吸器に移すときに特に重要です。 最初は興奮があり、次に精神障害と「呼吸パニック」があり、これは空気の不足感に関連しています。 将来的には、過敏性、混乱、無気力(昏迷と昏睡まで)が始まります。 呼吸性アシドーシスが発症します。 喘息状態の緊急治療 酸素療法。 湿った酸素が吸入される2 鼻カテーテルまたはマスクを介して、1〜2 l /分の速度で。 アドレナリンは、a1、b1、および b2 アドレナリン受容体を刺激し、気管支を拡張し、気道抵抗を減らします。 それは皮下に投与されます:体重が60kg未満の場合-0,3ml、体重が60〜80kgの場合-0,4ml、体重が80kgを超える場合-0,5ml。 Eufillin は、cAMP の蓄積と気管支痙攣の除去に寄与するホスホジエステラーゼを阻害します。 アミノフィリンを処方するときは、喫煙と小児期、心不全と急性冠症候群、肺、肝臓、腎臓の慢性疾患などの禁忌を考慮する必要があります。 AS では、アミノフィリンの負荷量は 3 ~ 6 mg/kg で、20 分かけて静脈内投与されます。 次に、合併症のない患者では0,6mg/kg/1時間、喫煙者では0,8mg/kg/1時間、うっ血患者では0,2mg/kg/1時間の割合で薬物の維持点滴を行う。心不全、肺炎 、肝臓および腎臓の疾患、重度の慢性肺疾患の場合、0,4時間あたり1 mg / kg。 コルチコステロイド療法の効果は、気道炎症の抑制とβ-アドレナリン薬に対する感受性の増加に関連しています。 AS が重症であるほど、即時のコルチコステロイド療法の適応が大きくなります。 高用量のコルチコステロイドを最初に投与する必要があります。 最小用量は、プレドニゾロン 30 mg またはヒドロコルチゾン 100 mg、またはデキサメタゾン (セレストン) 4 mg です。 治療が無効な場合は、用量を増やします。 少なくとも 6 時間ごとに、これらの薬剤の適切な同等量が投与されます。 ほとんどの患者は、β-アドレナリン作動薬による吸入療法を受けます。 (フェノテロール、アルペント、サルブタモール)。 交感神経刺激薬の薬物過剰摂取の場合は例外です。 進行中の治療で効果が得られない場合は、5% グルコース溶液で希釈したイソプロテレノールなどの β-アドレナリン作動薬の静脈内投与が必要です。 禁忌は、心臓病(冠状動脈硬化症、心筋梗塞)、重度の頻脈、頻脈の症状、老齢です。 イソプロテレノールの投与速度は、頻脈の発症まで0,1分あたり1μg/ kgです(130分あたりHR 1以上)。 点滴療法はASの治療の最も重要な要素であり、水分不足を補充し、循環血液量減少を排除することを目的としています。点滴療法の総量は3日あたり5〜0,30リットルです。 水和は、十分な量の遊離水を含む溶液(グルコース溶液)、ならびにナトリウムおよび塩素を含む低および等張電解質溶液を導入することによって実行されます。 適切な水分補給の指標は、喉の渇きの停止、舌の濡れ、正常な利尿の回復、喀痰の排出の改善、およびヘマトクリット値の0,40〜XNUMXへの低下です。 ハロタン麻酔は、従来の治療法では対応できない重度の喘息発作の治療に使用できます。 肺の人工換気。 AS患者の人工呼吸への移行の適応は非常に厳密でなければなりません。この状態では、合併症を引き起こすことが多く、死亡率が高いという特徴があるためです。 同時に、厳密な指示に従って実施された場合、機械的換気は、低酸素症と高炭酸ガス血症のさらなる進行を防ぐことができる唯一の方法です。 IVL の適応: 1)集中治療にもかかわらず、ASの着実な進行; 2) pCOの増加2 一連のテストによって確認された低酸素血症。 3) 中枢神経症状および昏睡の進行; 4) 疲労と疲労の増加。 粘液溶解薬と去痰薬は XNUMX つのグループに分けられます。 1. タンパク質分解酵素 (トリプシン、キモトリプシン) は、糖タンパク質のペプチド結合を切断することによって作用し、痰の粘性と弾力性を低下させます。 それらは粘液および化膿性の痰に効果的であり、抗炎症効果がありますが、喀血およびアレルギー反応を引き起こす可能性があります。 2.システイン誘導体は気管気管支樹(ムコソルバン、ムコミスト)の繊毛上皮の分泌活動を刺激し、20日2〜3回2〜3mlのXNUMX%溶液のエアロゾルとして使用されます。 講義 No. 6. 心臓病学における緊急事態 1. 心筋梗塞 心筋梗塞は、心筋の酸素需要とその送達との間の不一致であり、心筋の限定的な壊死をもたらします。 最も一般的な原因は血栓であり、塞栓症であることが少なく、冠状動脈のけいれんであることが少ないです。 血栓症は、冠状動脈へのアテローム性動脈硬化症の損傷を背景として最も頻繁に観察されます。 アテローム斑の存在下では、血流の渦巻きが発生します。 アテローム性動脈硬化症の病変は、脂質代謝の障害の結果として発症し、血液凝固が増加します。これは、ヘパリンを産生する肥満細胞の活動の低下に関連しています。 血液凝固と乱流の増加は、血栓の形成に寄与します。 アテローム斑の崩壊、それらの出血は血栓の形成につながる可能性があります。 素因は、男性の性別、50歳以上、肥満、遺伝、精神的感情的ストレス、勤勉です。 クリニックと診断 古典的に、心筋梗塞は胸骨の後ろの痛みが増すことから始まります。 腕(より多くの場合左)、背中、腹部、頭、左肩甲骨の下、左下顎などの痛みの広範な照射が特徴です。患者は落ち着きがなく、不安であり、時には恐怖感に気づきます死の。 心臓と血管の機能不全の徴候があります - 四肢の冷え、ベトベトした汗など。疼痛症候群は長引き、ニトログリセリンで 30 分以上緩和されません。 心拍リズムのさまざまな障害、血圧の低下または上昇があります。 患者は主観的に空気の不足感に気づきます。 上記の兆候は、痛みを伴うまたは虚血性の期間Iに典型的であり、その期間は数時間から2日間です。 客観的には、血圧の上昇(その後低下); 心拍数の増加またはリズム障害; 聴診では、異常な IV トーンが聞こえます。 心音がこもっている。 大動脈アクセント II トーンについて。 血液には実質的に生化学的変化はなく、心電図の特徴的な兆候です。 XNUMX番目の期間は急性(熱性、炎症性)で、虚血部位での心筋の壊死の発生を特徴としています。 痛みは通常消えます。 急性期の期間は最大2週間です。 患者の健康状態は徐々に改善しますが、全身の脱力感、倦怠感、頻脈が持続します。 心音がこもっている。 心筋の炎症過程による体温の上昇は、通常は38℃までで、通常は病気の3日目に現れます。 通常、最初の週の終わりまでに、気温は通常に戻ります。 血液を検査すると、白血球増加症、中等度、好中球性(10〜15千)、桿体への移行が見られます。好酸球が存在しないか、好酸球減少症です。 ESRの緩やかな加速; C 反応性タンパク質が表示されます。 トランスアミナーゼ活性の増加; 乳酸脱水素酵素、クレアチンホスホキナーゼ、およびその他の梗塞マーカーの活性の増加。 心特異的は、CPK-MB 画分と心筋トロポニンです。 4 番目の期間 (亜急性または瘢痕化) は 6 ~ XNUMX 週間続きます。 その特徴は、血液パラメーター(酵素)の正常化、体温の正常化、急性プロセスの他のすべての兆候の消失です。ECGが変化し、壊死部位に結合組織の瘢痕が発生します。 第6の期間(リハビリ期間、回復期間)は、1か月からXNUMX年続きます。 臨床症状はありません。 この期間中、無傷の心筋線維の代償性肥大が起こり、他の代償性メカニズムが発達します。 心筋機能の漸進的な回復がある。 しかし、病的な Q 波は心電図上に残ります。 しかし、臨床現場でよく見られる非定型の心筋梗塞の存在を忘れてはなりません。 これらには以下が含まれます。 1.腹部の形態は、吐き気、嘔吐を伴う腹部の剣状突起の下で、心窩部領域の痛みを伴う胃腸管の病状の種類に応じて進行します。 多くの場合、この形態(腹部)の心筋梗塞は、左心室の後壁の梗塞で発生します。 一般に、このオプションはまれです。 ECG は II、III、および VL を誘導します。 2. 喘息型は、心臓喘息の徴候を特徴とし、結果として肺水腫を引き起こします。 痛みがない場合もあります。 喘息型は、心臓硬化症の高齢者、再発性梗塞、または非常に大きな梗塞でより一般的です。 息切れ、窒息、咳があります。 肺の聴診 - 湿った微細な泡立つラレ。 3. 脳の形、または大脳。 同時に、前景では、意識喪失を伴う脳卒中のタイプによる脳血管障害の症状は、脳血管硬化症の高齢者でより一般的です。 めまい、吐き気、嘔吐、局所神経症状があります。 4. 無音または痛みのない形態は、健康診断中に偶然発見されたものです。 臨床症状のうち:突然「病気」になり、急激な衰弱、べたつく汗があり、その後、衰弱以外のすべてが消えます。 この状況は、高齢者の心臓発作や心筋梗塞を繰り返す場合に典型的です。 運動耐性のやる気のない低下が発生します。 5.不整脈の形態:主な症状は発作性-頻脈であり、痛みがない場合があります。 それは、心室性または上室性頻脈、房室ブロックII-III度、房室束の脚の急性遮断の兆候から始まります。 Morgagni-Adams-Stokes攻撃は、デビュー時に頻繁に発生します。 ほとんどの場合、心不整脈は、低血圧、不整脈性ショック、および急性心不全によって複雑になります。 心電図上の心筋梗塞の兆候は次のとおりです。 1)貫通性心筋梗塞または貫壁性(つまり、壊死ゾーンが心膜から心内膜に及ぶ)の場合:STセグメントが等値線より上に変位し、形状は「猫の背中」のように上に凸になります。 1〜3日目のT波とSTセグメントの融合。深くて広いQ波が主な兆候です。 R 波のサイズの減少、場合によっては QS 形式。特徴的な不調和な変化 - ST と T の逆のシフト(たとえば、第 1 の標準リードと比較した第 2 および第 3 の標準リード)。平均すると、3 日目から、ECG 変化の特徴的な逆ダイナミクスが観察されます。ST セグメントが等値線に近づき、均一な深い T が現れます。Q 波も逆ダイナミクスを受けますが、変化した Q と深い T は生涯持続する可能性があります。 ; 2)壁内または非貫壁性心筋梗塞の場合:深いQ波がなく、STセグメントの変位は上だけでなく下にもなる可能性があります。 心筋梗塞の診断の主な基準: 1) 臨床徴候; 2) 心電図の兆候; 3) 生化学的徴候。 合併症:心不整脈、房室伝導障害、急性左心室不全:肺水腫、心臓喘息、心原性ショック、胃腸障害(胃と腸の麻痺、胃出血)、心膜炎、壁側血栓心内膜炎、心筋破裂、急性および慢性心臓動脈瘤、ドレスラー症候群、血栓塞栓性合併症、梗塞後狭心症。 治療 治療は、合併症の予防、梗塞領域の制限、痛みの緩和、低酸素症の矯正を目的としています。 痛み症候群の除去:硝酸塩の摂取から始めます。 重度の低血圧では、神経弛緩痛が行われます - フェンタニル1〜2mlをブドウ糖で静脈内投与し、ドロペリドール0,25%を2%ブドウ糖溶液40mlあたり5ml。 効果が不完全な場合、モルヒネ 1% 1,0 は 2 時間後に皮下または静脈内に再導入されます。 omnopon 1,0% - 1 皮下または静脈内。 プロメドール 1,0% - XNUMX 皮下。 鎮痛効果を高めるために、不安、不安、覚醒を和らげ、適用します:筋肉内または静脈内に50%-2,0のアナルギン。 ジフェンヒドラミン 1% - 1,0 筋肉内 (鎮静効果) + クロルプロマジン 2,5% - 1,0 筋肉内、静脈内 (薬物増強)。 壊死のゾーンを制限するために、抗凝固剤が使用されます(ヘパリン5単位 - 1mlのボーラス、続いて1時間あたり6単位の注入ポンプの静脈内投与)、血栓溶解薬(フィブリノリシン250単位の静脈内点滴;ストレプターゼXNUMX千の生理食塩水中の静脈内点滴)および抗血小板薬(アスピリン、カルジオマグニル、血栓ACS、プラビックス)。 不整脈の予防と治療。 1.細胞へのカリウムの浸透を促進する分極混合物。 2. リドカインが最適な薬剤であり、心室性不整脈には 80 ~ 100 mg ボーラスでより効果的です。 3.生理食塩水中のコルダロンまたはアミオダロン450mgを静脈内投与。 心臓のポンプ機能が低下していることを考えると、b遮断薬(egilok 12,5-25 mg)の指定は、心収縮性を高めることが示されています。 下肢の浮腫または肺の湿ったラ音の存在下では、利尿薬が使用されます(40-80mgの用量のLasix)。 血圧に大きな重点が置かれ、血圧は低血圧(ドーパミン)で上昇するか、低下する必要があります(硝酸イソソルビド点滴、降圧薬-エナラプリル)。 低酸素症を解消するために、マスクまたは鼻カテーテルを通して加湿酸素を使用して酸素療法が行われます。 2.心原性ショック 心原性ショックは、動脈の低血圧と、臓器や組織の血液循環の急激な悪化の徴候を伴う重篤な循環障害です。 クリニックと診断 主な診断徴候は、収縮期血圧の大幅な低下であり、90 mm Hg を下回っています。 美術。 収縮期圧と拡張期圧の差(脈圧)は20mmHgです。 美術。 またはさらに小さくなる。 さらに、臓器や組織の灌流が急激に悪化している診療所が開発されています。 1) 軽度の無気力から精神病または昏睡までの意識障害、局所的な神経学的症状が現れることがあります。 2)20ml/h未満の利尿。 末梢循環の悪化の症状:青白いチアノーゼ、大理石、レンガ、湿った皮膚。 末梢静脈の虚脱、手足の皮膚温度の急激な低下; 血流の減少。 CVP の値は異なる場合があります。 CVP の通常の指標は 5 ~ 8 cm の水です。 美術。; 水深 5 cm 以下のインジケータ。 美術。 循環血液量減少と低血圧、および 8 cm 以上の水を示します。 美術。 右心室不全を示します。 通常、心原性ショックの診断は難しくありません。 そのタイプと主要な病態生理学的メカニズムを特定することはより困難です。 まず第一に、真の(収縮性)心原性ショックと、不整脈、反射性(痛みを伴う)、右心室不全またはゆっくりと進行する心筋破裂による医学的ショックを区別する必要があります。 ショック患者の集中治療を行う際には、血液量減少、心タンポナーデ、緊張性気胸、血栓塞栓性合併症などの低血圧の原因を除外し、ストレスによるびらんや潰瘍などの内出血を見逃さないことが重要です。消化管。 治療 マスクまたは鼻カテーテルを介した加湿酸素による酸素療法が必要です。 抗凝固剤を 10 IU の用量でボーラスとして投与した後、000 時間あたり 1000 IU で注入ポンプを静脈内投与します。 鎮痛剤を投与する必要があります:モルヒネ1%1,0mlを皮下またはボーラスで静脈内投与。 アナルギン50%2mlを筋肉内、静脈内に。 血管強壮剤:コルジアミン1~4mlの静脈内投与。 メザトン 1% 1,0 g 皮下、静脈内、生理食塩水中。 ノルエピネフリン 0,2% 1,0 静脈内投与。 真の心原性ショックは次のように治療されます。 心筋の収縮活性を高めるために、以下が使用されます:ストロファンチン0,05%0,5〜0,75 gを20,0等張液あたりゆっくりと静脈内投与、コルグルコン0,01 gを静脈内投与、また等張液または分極混合物中、グルカゴン2〜4 mgを静脈内投与偏光溶液に滴下します。 血圧の正常化:0,2%グルコース溶液または等張液2リットルあたりノルエピネフリン4%1〜5ml。 血圧は100mmHgに保たれています。 Art.、メザトン 1% 1,0 g 静脈内投与。 コルジアミン 2-4 ml、ドーパミン 200 mg を 400 ml のレオポリグルシンまたは 5% グルコースに溶解。 上記の薬による不安定な効果により、ヒドロコルチゾン200mg、プレドニゾロン90〜120mgが使用されます。 血液のレオロジー特性の正常化(微小血管血栓が必然的に形成されるため、微小循環が妨げられます)。 血液の液体部分が発汗しているため、血液量減少の解消:レオポリグルキン、ポリグルキン - 毎分100mlの速度で最大50,0mlの量。 酸塩基バランスの修正(アシドーシスとの戦い):重曹5%から200,0ml。 鎮痛剤の再導入。 リズムと伝導障害の回復。 しかし、CVPを制御することは常に必要であり、これにより蘇生者は許容可能な注入療法を決定することができます。 心原性ショックの患者は水を入れてはいけません。 CVPが高いほど、点滴療法は少なくなります。 3. 高血圧クリーゼ 高血圧クリーゼとは、通常はこの患者に特徴的ではないレベルまで血圧が急激に上昇し、急性の局所循環障害と標的臓器 (心臓、脳、腎臓、腸) の損傷につながるものです。 危機を引き起こす外部要因には、次のようなものがあります。 1) 精神的ストレス; 2) 気象の影響。 3) 食卓塩の過剰摂取。 春と秋には、冬と夏よりも危機が頻繁に発生します。 危機は、多くの慢性疾患の悪化を背景に発生する可能性もあります。 MS Kushakovsky (1982) は、高血圧クリーゼの次の変種を特定しています: 神経栄養、水-塩、痙攣 (脳症)。 診療所 危機の臨床症状は、耳鳴り、目の前でのハエの点滅、後頭部の破烈な頭痛、かがみ込み、いきみ、咳、吐き気、嘔吐、および心拍リズムの乱れによって悪化します。 危機の間、脳冠動脈の危険な違反、腎臓および腹部循環の頻度が少なくなり、脳卒中、心筋梗塞およびその他の深刻な合併症につながります。 心電図は左心室肥大を明らかにします。 胸部 X 線では、肋間動脈を通る側副血行の増加の結果として、拡大した心臓、数字「3」の形の大動脈変形、肋骨の高利貸しが示されます。 大動脈造影により診断が確定します。 神経栄養型の危機は、突然の発症、興奮、皮膚の充血および水分、頻脈、頻繁な大量排尿、脈拍振幅の増加を伴う収縮期圧の顕著な増加によって特徴付けられます。 このような危機は、副腎の危機、またはタイプ I の危機と呼ばれます。 タイプ I の危機は、発作性不整脈や狭心症、重篤な場合には心筋梗塞を引き起こす可能性がありますが、通常は比較的良性の経過をたどります。 発症の水塩形態では、状態は徐々に悪化し、眠気、衰弱、無気力、見当識障害、顔面蒼白および腫れ、および腫れが認められる. 収縮期圧と拡張期圧は均等に、または後者が優勢で脈圧が低下して増加します。 このような危機は、タイプ II の危機と呼ばれます。 タイプIIの危機は、原則として深刻であり、心筋梗塞、脳卒中、急性左心室不全によって複雑になる可能性があります。 特に、β遮断薬、ニフェジピン、交感神経遮断薬、特にクロニジンの服用など、永続的な降圧療法の突然の中止の結果として発症する高血圧クリーゼを強調する必要があります。 治療 高血圧クリーゼの治療は、高血圧症の標的臓器への損傷を予防または制限するために必要な正常レベルへの血圧の緊急の低下、最も重度の症例での死亡に至るまでの合併症の予防、または脳卒中の発症における永久的な障害からなる。 、心筋梗塞。 神経栄養型の危機では、通常、静脈注射、0,1 mg のクロニジンのゆっくりした投与、または 50 mg のラベタロールの反復静脈内注入が使用されます。 クロニジンの降圧効果は、10 mg のニフェジピンの舌下投与によって強化できます。 非常に重度の場合、ニトロプルシドナトリウムが静脈内に注射され、それがない場合は、点滴または非常にゆっくりと、ペンタミン50mgまで注射されます。 降圧療法の主な危険性と合併症: 1) 動脈性低血圧; 2)脳循環の侵害(出血性または虚血性脳卒中、脳症); 3) 肺水腫; 4)狭心症、心筋梗塞; 5) 頻脈。 生命を脅かす高血圧クリーゼは、即時集中治療の根拠です。 高血圧クリーゼの種類. 1.高血圧クリーゼの痙攣型(急性重度高血圧性脳症)。 2.褐色細胞腫の危機。 3.生命を脅かす疾患および状態における急性動脈性高血圧(急性冠症候群、急性心筋梗塞、解離性大動脈瘤、内出血)。 4. 肺水腫または出血性脳卒中を合併した高血圧クリーゼ。 痙攣型の高血圧クリーゼ(急性重症高血圧性脳症)は、悪性型の高血圧症または二次性動脈性高血圧症、たとえば妊婦の晩期中毒症または急性糸球体腎炎で発症します。 危機は、重度のズキズキ、アーチ型の頭痛、精神運動性興奮、緩和をもたらさない反復嘔吐、視覚障害から始まります。 意識消失が急速に起こり、間代性強直性痙攣が現れる。 最近の動脈性高血圧症(急性糸球体腎炎、妊娠中の女性の中毒症)の患者では、血圧の比較的わずかな上昇で痙攣性高血圧クリーゼが発生することがあります。 けいれん型の危機では、救急医療は、けいれん症候群と緊急の血圧低下をなくすことを目的としています。 痙攣症候群は、ジアゼパムの静脈内投与によって排除されます。 さらに、硫酸マグネシウムの10%溶液25 mlを点滴または徐流により静脈内投与するか、筋肉内投与することができます。 ニトロプルシドナトリウム、ラベタロール、ジアゾキシドは、緊急に血圧を下げるために使用されます。 脳浮腫と戦うために、ラシックスの静脈内ジェット投与が適応とされています。 子癇、特に静脈内投与では、硫酸マグネシウムが依然として広く使用されており、4%ブドウ糖溶液100mlあたり5gの用量で投与されます。 次に、必要に応じて、薬物の点滴注射を行うか、またはその後の硫酸マグネシウムの点滴注射の代わりに、硫酸マグネシウムの20%溶液25mlを筋肉内に深く注射することができる。 妊娠中の女性がカルシウム拮抗薬で治療されている場合は、硫酸マグネシウムの静脈内投与は避ける必要があります(血圧の急激な低下は危険です)。 おそらく子癇とクロルプロマジン(100-250mg)、ジアゾキシド(300mg)の静脈内投与を伴う。 セデュクセン(ジアゼパム)はゆっくりと静脈内投与され(20-30 mg)、その後点滴されます(300 mlの500%ブドウ糖溶液に5 mg)。 褐色細胞腫の発症は、主に収縮期の血圧の突然の非常に急速かつ急激な上昇、および脈圧の上昇によって現れ、淡い肌、冷汗、動悸、心臓および心窩部の痛み、吐き気、嘔吐を伴います、ズキズキする頭痛、めまい。 危機の間、体温の上昇、視覚および聴覚障害が発生する可能性があります。 垂直姿勢への移行後の血圧の低下が特徴です。 褐色細胞腫を伴う危機の場合の救急医療は、ベッドのヘッドエンドを45°の角度に上げることから始まります。これにより、血圧が低下します。 緊急降圧療法の場合、選択される薬剤はフェントラミンであり、5分ごとに5mlの流れで静脈内投与されます。 同じ目的で、50分ごとに5mlのラベタロールを静脈内注射するか、30mlの300%グルコース溶液に5mlのニトロプルシドナトリウムを点滴注入します。 追加の薬として、ドロペリドール(5-10 ml IV)が有用かもしれません。 頻脈を抑制するために、プロプラノロールは20〜40mgの用量で処方されます。 急性心筋梗塞(特にその前方局在化でしばしば指摘される)では、危機の間に心筋への負荷が増加し、心筋酸素需要が増加すると、最初に現代の鎮痛剤(麻薬性鎮痛薬を含む)の助けを借りて激しい痛みの発作を止める必要があります) 血圧を大幅に下げることができる鎮静剤を投与します。 重大な高血圧が持続し、同時に交感神経系の緊張が高まる場合、bブロッカー(プロプラノロール、メトプロロール、エスモロール)が静脈内投与され、血圧降下作用とともに、周囲の領域を制限する可能性があります・梗塞心筋虚血。 多くの場合、ニトログリセリンの静脈内投与に頼って、前負荷と後負荷を減少させます. これにより、血圧のレベルを制御できます。 ただし、ニトロプルシド ナトリウムの指定は避ける必要があります。これらの場合、明らかに「冠動脈盗用」(虚血帯への冠動脈側副血流の減少) の現象により、心筋虚血が増加する可能性があります。 心筋梗塞の急性期の後に高血圧が持続する場合は、適応症と禁忌を考慮して、主要な降圧薬による治療が開始されます。 しかし、近年、二次予防に関するデータに関連して、b遮断薬とACE阻害薬が最も好まれており、禁忌がない場合は、早期から処方されることが試みられています。 急性心不全の発症に伴い、高血圧の危機はニトログリセリンの静脈内投与によって停止します(重度の僧帽弁狭窄症には禁忌)。 血管拡張剤を処方します(耐性がしばしば発達しますが)、IFKA。 重度の心不全の場合の持続性高血圧症では、利尿薬との組み合わせが必要であり、少量のサイアザイド利尿薬とカリウム保持性利尿薬(トリアムテレンまたはアミロライド)を併用するだけで、血圧を正常化するだけでなく、発生を防ぐこともできますそのような患者のカリウムおよびマグネシウム欠乏によって引き起こされる不整脈の。 (Metelitsa V.I.、1996)。 出血性脳卒中またはくも膜下出血では、降圧効果を簡単に制御できる薬(ニトロプルシドナトリウム)の助けを借りて、通常よりも高いレベル(作用)まで、特に慎重に血圧を下げる必要があります。 神経学的状態の悪化を伴う血圧の低下は、過剰と見なされるべきです。 肺水腫の場合、ニトログリセリンまたはニトロプルシドナトリウムまたはペンタミン、ならびにラシックスは、緊急に血圧を下げるために静脈内に処方されます。 解離性大動脈瘤または破裂では、次の薬が静脈内に使用されて血圧を調節し、外科的治療に備えます:ニトロプルシドナトリウム、ループ利尿薬(フロセミド)、ニフェジピン、プロプラノロール(ニトロプルシドナトリウムとともに)、メチルドパ、レセルピン(追加エージェント)。 心拍出量の増加によって引き起こされる危機では、頻脈と収縮期および脈圧の主な増加がしばしば観察されます。これらの場合の良い効果は、アナプリリン、次に必要に応じてフロセミドの静脈内投与です。 4.生命を脅かす不整脈 不整脈 不整脈は、洞以外の心臓のリズムです。 正常な心臓のリズムには、次の特徴があります。 1) 毎分60から120までの心拍数; 2) ペースメーカーは洞結節であり、その証拠は、標準誘導 II では QRS 群に先行する正の P 波であり、AVR では負です。 3)RR間隔の差は0,01秒以内です。 4)標準の間隔と歯のサイズを反映した実際の指標。 ECG のすべての変更は、II 標準リードで実行されます。 不整脈の分類 1.衝動の形成の違反: 1) 洞結節: a)洞性頻脈; b) 洞性徐脈; c)洞不整脈; d) 洞不全症候群 (SSS); 2)異所性不整脈: a) 期外収縮; b) 発作性頻脈; c) 心房細動および粗動; d) 心室のフリッカーとフラッター。 2. インパルス伝導の違反: 1) 追加の経路 (Kent バンドル); 2) 心臓ブロック: a) 心房 (心房内); b)房室; c) 脳室内。 不整脈のメカニズム 静止電位の低下、興奮性閾値は、細胞カリウムの欠乏、「血漿 - 細胞」の比率に基づいてのみ発生します(通常、カリウムの80 meqは細胞内にあり、5 meqは血漿内にあります). 血栓溶解中の虚血、炎症、再灌流による心筋の電気生理学的代謝焦点の非対称性。 上位ペースメーカーの電気生理学的脱力。 先天性副伝導経路。 発作性上室性頻脈 発作性上室性頻脈は、毎分 150 ~ 250 回の心拍数の突然の発作です。 3 つの形式があります。 1) 心房; 2) 結節; 3) 心室。 上室性発作性頻脈の病因は、交感神経系の活動の増加と関連していることが多い。 それは、心拍の突然の攻撃、首の血管の脈動、心臓の活動が異なるリズムに切り替わることによって臨床的に現れます。 攻撃の持続時間は数分から数日です。 心室型の心拍数は通常、毎分 150 ~ 180 回の範囲であり、上室型の場合は毎分 180 ~ 240 回です。 攻撃中、振り子のようなリズムが特徴的な聴診器であり、I トーンと II トーンに違いはありません。 それは心筋の酸素需要を増加させ、急性冠動脈不全の発作を引き起こす可能性があります。 心電図の兆候 1. QRS コンプレックスは変更されません。 2. 上室型では、P 波が T 波と合流します。 治療は、コルダロンを300 mgまたはノボカインアミドを最大1 gの用量で静脈内投与し、次にアデノシン1 ml - 1%(10 mg)ボーラスを静脈内投与することから始まります。 カルシウム拮抗薬のベラパミル(イソプチン)は、2,5~5分かけて2~4mgの用量でボーラスとして静脈内に使用されます。 しかし、それは狭い QRS 群に使用され、幅の広い QRS 群では線維化する可能性があります。 bブロッカー(プロプラノロール20〜40mgを舌下)を服用することは可能です。 心房細動の発作 心房細動の発作は、心房複合体の欠如によって特徴付けられ、等値線の代わりに、心房粗動の鋸歯状波が検出されます。これは、250 ~ 400 拍/分の周波数の誘導 II、III、および VF で最も顕著です。 または、心房複合体がなく、ちらつき波、アイソラインの大波または小波の振動が検出され、心房波の周波数は毎分350〜600拍です。 診療所。 脈拍は不整脈で、さまざまな充填の波、脈拍欠損の存在(心拍数と脈拍の差)があります。 聴診中の心音の異なる間隔と異なる音量。 処理。 発作の場合は、生理食塩水 0,25ml あたりジゴキシン 1mg(0,025% 20ml)をボーラス静注することから始める。 配糖体による飽和の望ましい効果を達成するには、1,5 日または 3 日あたり XNUMX mg のジゴキシンの用量が推奨されます。 合併症のない発作の場合、選択される薬剤はノボカインアミドであり、血圧、心拍数、ECGを常に監視しながら、最大2000 mlの用量で30分間かけてゆっくりと静脈内投与されます(10%溶液10 ml)。 心房粗動は電気インパルス療法で治療されます。 発作性心室頻拍 発作性心室性頻拍は、3分間に0,12~100回の頻度で250つ以上連続した幅の広い(XNUMX秒以上)QRS群が検出されることを特徴とし、STセグメントとT波が逆方向に不一致にシフトします。 QRSコンプレックスのメインウェーブ。 ピルエット、または双方向の紡錘状心室頻脈は、QT間隔が長くなると発生します。この場合、不整脈は、幅の広い多形変形QRS群で150分あたり250〜1拍の心拍数で記録されます。 処理。 血液循環の低活動状態では、電気パルス療法が必要です。その後、リドカインの点滴で支持療法が行われます。 血行動態が安定している状態では、最適な薬剤はリドカインであり、1~2 mg/kg (80~100 mg) を 3~5 分間静脈内ボーラスで投与した後、日中は 4 mg/分で点滴します。 心室性期外収縮 心室性期外収縮は、異常に大きく変形したQRS群、不一致のSTおよびTシフト、完全な代償性休止の発生です(収縮期外P波の前後の間隔は通常のRR間隔の300倍に等しい)。 選択される薬はリドカインであり、これは上記のスキームに従って投与されます。 おそらく、450-XNUMXmgの用量でのコルダロンの静脈内点滴の使用。 失神の発症を伴う房室伝導障害(モルガニ・アダムス・ストークス症候群) 伝導が妨げられると、さまざまな種類の心ブロックが発生し、心臓の伝導系を介したインパルスの伝導が遅くなるか完全に停止します。 洞耳遮断は、T細胞の機能不全および洞結節から心房へのインパルス伝導障害を特徴とする。 3度あります。 私は程度-衝動を遅くします。 ECGについて-0,20秒を超えるPQ間隔の延長。 QRS群の脱出。 RR間隔は安定しています。 II度 - インパルスの一部の損失、不完全な伝導。 Mobitz タイプ I - インパルスが実行されると、脈波が完全に失われるまで PQ 間隔が徐々に長くなります。 QRS は変更されません。 QRS 脱出部位での最大距離は RR です。 予後的に、このタイプは比較的有利です。 一定の PQ 間隔と変更されていない QRS 群を持つモビッツ II 型。 同時に、すべてのインパルスが心室に到達するわけではありません-場合によっては、3回ごとのインパルスが実行され、他の場合-2回ごとなど、つまり、QRS群の周期的な脱出があります4:3、5:6 、XNUMX:XNUMX など d. III度 - 伝導の完全な遮断。 同時に、心室へのインパルスの伝導は完全に停止し、心室では心室リズムの異所性焦点が生まれ、自動化が低いほど診療は困難になります。 完全な解離が観察されます。心房のリズムは正常に近く、心室には独自の周波数があります-毎分40拍以下です。 後者は損傷のレベルに依存します。AVノードが苦しんでいる場合、40分間に50〜1拍、ヒスの束の脚が20分間に1拍以下の場合です。 損傷のレベルは、QRS群の変形の程度によっても示されます。 心房と心室の収縮期がほぼ一致すると、心音が弱まり、定期的に「大砲」のIトーンが鳴ります。 III追加トーンかもしれません。 収縮期の心雑音が心臓の基部に現れることがあります。 多くの場合、心房収縮に関連する静脈の脈動が見られ、特にストラジェスコの大砲の緊張とは異なります。 診療所。 一つの衝動が抜ければ心の衰え。 いくつかの衝動が落ちる場合のめまい。 モルガニ・アダムス・ストークス症候群(意識喪失)、6〜8個の複合体が脱落した場合。 処理。 適切なリズムを回復するために、アトロピンは0,5〜1mgから3mgの用量で投与されます。 3分ごとに、1mgから総投与量0,4mg/kg。 カルシウム拮抗薬-イソプチン0,04mg/kg。 意識が頻繁に失われると、患者は永続的な電気パルス療法に移行します。 しかし、多くの場合、ペーシングは「オンデマンド」で実行する必要があります。 講義番号7.急性腎不全 急性腎不全(ARF)は、腎機能の急激な悪化または停止を特徴とする多くの腎疾患および腎外疾患の合併症であり、以下の複合症状によって現れます:乏尿、高窒素血症、水分過剰、CBSおよび水分と電解質のバランスの障害。 OOP の形式には次のものがあります。 1) 腎前 (血行動態); 2) 腎臓 (実質); 3) 腎後 (閉塞性); 4) アレナル。 病因 腎前性急性腎不全の発症の理由。 1.心拍出量の減少(心原性ショック、発作性不整脈、心タンポナーデ、肺塞栓症、うっ血性心不全)。 2.血管緊張の低下(敗血症、感染性毒素性ショック、アナフィラキシーショック、降圧薬の過剰摂取)。 3.有効血管内容積の減少(失血、血漿喪失、脱水 - 体重の7〜10%の喪失、大量の嘔吐、下痢、多尿、妊娠中の腎症を伴う血液量減少、ネフローゼ症候群、腹膜炎、肝硬変)。 4.腎内血行動態の違反(NSAID、ACE阻害薬、放射線不透過性薬、砂免疫薬の服用)。 5.水中毒 - 水分過剰(悪性腫瘍、中枢神経系の炎症性疾患、薬物過剰摂取 - 薬物、バルビツレート、抗糖尿病性スルファニルアミド薬、インドメタシン、アミトリプチリン、シクロホスファミドにおける制御不能なADH産生)。 腎性急性腎不全の発症の理由。 1.腎臓の虚血(ショック、脱水症)。 2.以下への曝露による腎毒性損傷: 1) 薬物 (アミノグリコシド、NSAID、放射線不透過性薬剤、スルホンアミド、フェナセチン、バルビツレート、セファロスポリン、アンピシリン、リムファピシン、サンディミューン); 2)工業用ネフロトキシン(重金属の塩:水銀、クロム、カドミウム、鉛、ヒ素、プラチナ、ビスマス、金、ウラン、バリウム); 3)家庭用ネフロトキシン(エチレングリコール、メチルアルコール、ジクロロエタン、四塩化炭素)。 3.色素による尿細管内閉塞: 1)ヘモグロビン(溶血 - 不適合輸血、きのこ中毒、酢酸、溶血性貧血、溶血性尿毒症症候群、血栓性血小板減少性紫斑病); 2) 尿酸塩 (痛風、多発性骨髄腫および白血病の免疫抑制療法、激しい身体活動、暑さに適応していない人々); 3)ミオグロビン(外傷性横紋筋融解症、昏睡状態の非外傷性横紋筋融解症、電気的損傷、凍傷、子癇、アルコール性およびヘロインミオパシー、重度の低カリウム血症および低リン血症、一酸化炭素中毒、水銀塩、亜鉛、銅、薬物、ウイルス性筋炎、過剰摂取スタチンおよびフィブラート); 4) 炎症過程: 薬用および感染症発生の OTIN (AIDS、HFRS、麻疹、単核球症、レプトスピラ症、マイコプラズマ症、リケッチア症) 急性腎盂腎炎、急性糸球体腎炎; 5) 壊死性乳頭炎 (真性糖尿病、鎮痛剤、アルコール性腎症); 6)血管の病理(血管炎 - 結節性多発動脈炎、ウェゲナー肉芽腫症、全身性強皮症、動脈または静脈血栓症、両側腎動脈塞栓症、外傷)。 腎後急性腎不全の発症の理由。 1. 尿管の病理: 1)閉塞(結石、血栓、壊死性乳頭炎); 2)圧迫(骨盤臓器の腫瘍、後腹膜線維症)。 2. 膀胱の病理 (結石、腫瘍、膀胱頸部の炎症性閉塞、前立腺腺腫、脊髄病変における神経支配障害および糖尿病性神経障害)。 3. 尿道狭窄。 分類 E. M. TareevによるOPN分類。 1.ショック腎臓。 2. 有毒な腎臓。 3.急性感染性腎臓。 4.血管閉塞。 5.泌尿器科の腎臓。 急性腎不全の経過の選択肢:周期的、再発性および不可逆性。 診療所 急性腎不全の臨床経過には XNUMX つの段階があります。 急性腎不全のステージ I は初期段階であり、病因因子が発生した瞬間から最初の徴候が現れるまで続きます。 この段階では、治療戦術は、病因要因の影響を排除または軽減することを目的としています: 抗ショック療法、BCC の補充、心不全との闘い、血管内溶血のためのアルカリ化療法、痛みとの戦い、敗血症状態の治療など。治療、毎時利尿の制御下で腎血管のけいれんが解消されます。 利尿刺激の開始が早ければ早いほど、予後は良好です。 急性腎不全のステージ II、またはオリゴ無尿症は、ネフロンの 70% の機能不全によって特徴付けられます。 排尿量が 500 日あたり 50 ml 未満の場合は、乏尿の発生を示し、XNUMX 日あたり XNUMX ml まで減少します。 以下は無尿を示す。 腎臓の水分排出能力の侵害に加えて、濃度と窒素排出機能も損なわれます。 尿では、電解質と窒素の量が急激に減少します。 この段階で、止血の最も顕著な変化が起こります。 治療は、腎臓上皮が再生する時間と機会を与えるために、一定の内部環境を維持することを目的とすべきです。嘔吐や下痢による電解質の喪失により、過水症状態が発生します。したがって、中心静脈圧の制御下でのみ利尿を刺激する必要があります。腎臓の血流を改善します。利尿を厳密にコントロールする必要があるため、膀胱カテーテル治療が行われます。腎臓の窒素排泄機能の低下は高窒素血症を引き起こすため、体内のタンパク質の分解を最大限に防ぐためには、十分な量の炭水化物(5日あたり少なくとも2 g/kg)を導入する必要があります。果糖とブドウ糖を2:1:1の割合でキシリトール(ソルビトール)を加え、果糖がない場合はブドウ糖3部、ソルビトール1部を加えます。経過が重度で治療できない場合は、血液透析セッションが行われます。病因が除去されると、治療の1〜1日後に利尿が増加し始めます。この段階の最長期間は最大 3 週間です。 急性腎不全のIII期 - 初期の多尿。 利尿作用が徐々に増加し(200 日あたり 300 ~ 3 ml)、最大 XNUMX リットルまで増加することが特徴です。 腎臓の窒素排泄・濃縮機能はまだ完全には回復していませんが、カリウム、マグネシウム、リン酸塩の濃度は徐々に正常化しています。 初期の多尿段階における集中治療には、利尿の刺激を除いて、前のものと同じ措置を含める必要があります。 多くの場合、血液透析が必要です。 脱水のリスクが高いです。 急性腎不全のIV期-後期多尿症。 尿の500日あたりの増加は1000〜8 mlに達し、利尿は10日あたりXNUMX〜XNUMXリットル以上に達する可能性があります。 腎臓では、イオン交換プロセスが回復し始めます。 カリウム、マグネシウム、リン、その他の電解質の喪失が急激に増加し、患者は脱水症や脱灰のリスクにさらされています。 したがって、電解質と水分はこの段階で静脈内投与されます。 ステージ V OPN、または回復ステージ。 腎臓の集中機能が回復します。 利尿は徐々に正常に減少し始め(2日あたり3〜1008リットル)、尿密度が増加します(1028〜XNUMX). 病気の重症度と治療の有効性を判断するために、急性腎不全の患者は、CBS、電解質の濃度、ヘモグロビン、糖、総タンパク質とタンパク質画分、尿素、残留物、尿素窒素の指標について血液中で毎日検査されます、クレアチニン、ヘマトクリット、および毎日の尿中-密度、電解質と窒素の量。 治療 治療の原則は次のとおりです。 1.ショックの治療:抗ショック対策、グルココルチコステロイド。 2. BCCの補充:ポリグルシン、レオポリグリキン、血漿、アルブミン、赤血球量。 3.感染症の治療:適切な抗生物質療法。 4.脱水症:塩化ナトリウム、ブドウ糖の等張性、高張性、低張性の溶液。 5.毒による中毒:解毒剤が導入されます。 6. 泌尿器の腎臓: 閉塞の除去。 7.尿細管内閉塞:最大60時間の集中注入アルカリ化療法(マンニトール10%溶液3〜5 ml / kg / h、等張塩化ナトリウム溶液、重炭酸ナトリウム、グルコース400〜600 ml / h、フロセミド30〜50 mg / kg)。 8.腎血管のけいれんの除去:ユーフィリン2,4% - 10〜4時間後に再び6ml、チャイム0,5% - 2〜4〜6mlの静脈内投与、トレント3〜5mg / kg /日、ペンタミン0,5〜1,0mg /kg/日、ベンゾヘキソニウム 0,3-0,5 mg/kg/日、ドロペリドール 0,12 mg/kg/日、ドーパミン 1,5-3 mg/kg。 9.利尿の刺激(血圧の安定化と循環血液量減少の除去後):アミノフィリン、マンニトール、ラシックス。 10. XNUMX時間ごとの利尿、血圧、CVPの管理。 急性血液透析の適応症:過異化性急性腎不全、非異化性急性腎不全における保存療法の効果が2~3日間欠如している、6~6,5mmol/l以上の高カリウム血症、15以上の塩基欠乏を伴う非代償性代謝性アシドーシスmmol/l、血中クレアチニンが 600 µmol/l 以上、血中尿素が 30 mmol/l 以上、肺水腫または脳浮腫の発症を伴う水分過剰。 講義番号8。急性肝不全。 急性肝不全は、実質への急性または慢性の損傷によるXNUMXつまたは複数の肝機能の侵害を特徴とする複合症状です。 病因 急性腎不全の原因は、A型、B型、C型、D型、E型、G型肝炎ウイルス、ヘルペスウイルス、サイトメガロウイルス、伝染性単核症ウイルス、帯状疱疹、コクサッキー、麻疹、肝膿瘍を伴う敗血症などです。化膿性胆管炎、薬物、アルコール、産業毒素、心不全。 OPN は常に複数の臓器の損傷を伴って進行します。この過程には、腎臓、心血管系、肺、膵臓、および脳が関与しています。 腎機能障害は、急性尿細管壊死として現れます。 肺合併症 - 胃内容物または血液の誤嚥、無気肺、呼吸器感染症。 急性膵炎および膵臓壊死は死に至る可能性があります。 生命を脅かすホメオスタシスの障害が発生します。 肝不全は、肝細胞のジストロフィーおよび広範な壊死によって説明される。 クリニックと診断 ARFの臨床症状は以下の通りです。 1.凝固障害は、凝固因子の欠乏と線維素溶解活性の増加によって引き起こされます。 粘膜からの特発性出血の素因となります:胃腸、子宮、鼻出血が観察されます。 脳出血の可能性があります。 止血システムの状態を評価するために、プロトロンビン時間が決定されます。 2. 低血糖症は、血漿中の高レベルのインスリンによって特徴付けられます。これは、肝臓による取り込みの減少によるものです。 それは神経学的状態の急速な悪化と患者の死につながります。 3. 水 - 電解質と酸 - 塩基バランスの違反。 末期急性腎不全は、低ナトリウム血症、低リン血症、低カルシウム血症、および低マグネシウム血症を特徴としています。 酸塩基状態の変化には明確な方向性はありません。 毒性物質による呼吸中枢の刺激に関連する呼吸性アルカローシスは、頭蓋内圧の上昇と呼吸活動の抑制による呼吸性アシドーシスに置き換わる可能性があります。 疾患の重篤な経過としての肝性昏睡の発症において、前昏睡、脅迫的昏睡および昏睡の段階が区別される。 顕著な門脈吻合の存在による代謝プロセスからの肝臓の有意な排除による、実質、門脈(バイパス、シャント、外因性)の大規模な壊死に起因する肝細胞性(内因性)昏睡もあります。主に肝硬変で起こる混合昏睡。 昏睡前の期間には、進行性の食欲不振、吐き気、肝臓のサイズの減少、黄疸の増加、高ビリルビン血症、および血中の胆汁酸の含有量の増加が発生します。 将来的には、神経精神障害、思考の鈍化、うつ病、そして時には陶酔感が増加します。 気分の不安定さ、過敏性、記憶障害、睡眠障害が特徴です。 腱反射が増加し、手足の小さな震えが特徴的です。 高窒素血症が発症します。 タイムリーな治療により、患者はこの状態から抜け出すことができますが、肝臓に深刻な不可逆的な変化が生じると、昏睡が発生することがよくあります。 昏睡状態の期間中、興奮が起こり、それはその後、うつ病(昏迷)と完全に失われるまでの進行性の意識障害に置き換わります。 髄膜現象、病的反射、運動不穏状態、けいれんが発生します。 呼吸が妨げられている(クスマウル、チェーンストークスなど)。 脈拍は小さく、不整脈です。 低体温症があります。 患者の顔はぎこちなく、四肢は冷たく、口や皮膚から特徴的な甘い肝臓の匂いがし、出血現象が激しくなります(皮膚の出血、鼻からの出血、歯茎、食道の静脈瘤など)。 急性肝不全は、数時間または数日以内に急速に発症し、タイムリーな治療により元に戻すことができます. 臨床検査:血液および尿中のビリルビン、尿素およびクレアチニン、止血システムのパラメーター、完全な血中数および尿、CVP、ECG、血漿および尿浸透圧、血漿電解質、遊離血漿および尿ヘモグロビン、ALT、AST、アルカリホスファターゼ、 LDH、CPK、プロトロンビン時間。 肝臓のコンピューター断層撮影はそのサイズの減少を明らかにすることができますが、ほとんどの臨床医は臨床および実験データに焦点を合わせています。 治療 タイムリーな変力作用のサポートは、集中治療に不可欠な要素です。 感染性合併症の予防 - 抗真菌薬(アムホテリシン-B)と組み合わせたセファロスポリン抗生物質の指定。 肝保護剤および膜安定化薬:プレドニゾロン最大300mg、ビタミンC 500mg、トロキセバシン5ml、エタムシル酸ナトリウム750mg、エッセンシャル30ml、トコフェロール4ml筋肉内、サイトマック35mg、コカルボキシラーゼ300mg、ニコチン酸30-40mg、コンプラミン 900 mg、シレパー 5-10 ml、グルタミン酸 1% 400 ml、ビカソル 10 ml 静脈内投与、ビタミン B。 皮質の100万単位、トラシロール400万単位、アンタゴノサン、ゴルドックスを含むプロテアーゼ阻害剤。 利尿の刺激: レオグルマン 400 ml、マンニトール、ラシックス 200 mg まで静脈内投与、ユーフィリン 240 mg。 凝固障害を是正するために、ビタミンKの静脈内投与(10日3mgを3日間)が使用されます。 効果は1時間後に発生します.この場合、胆汁酸の欠乏に起因するビタミンKの吸収障害に関連する低プロトロンビン血症の解消. 出血または侵襲的処置(血管カテーテル法、腹膜透析)が疑われる場合、血小板塊または新鮮凍結血漿が静脈内投与されます。 脳浮腫は一般的な死因です。 マンニトールは、体重1kgあたり1gの割合で投与される。 腎不全の患者では、高浸透圧と水分過剰を避けるために、限外濾過と組み合わせてマンニトールが処方されます。 肝性昏睡の発症に伴い、塩化カリウム(0,4mlの容量の0,5%グルコース溶液中5〜500%溶液を静脈内点滴)または重炭酸ナトリウム溶液(代謝性アシドーシスを伴う)が処方されます。 患者は、鼻カテーテルを通して加湿酸素を呼吸します。 動脈圧と静脈圧の両方が低下すると、ポリグルシンとアルブミンが静脈内投与されます。 大量の出血がある場合は、適切な対策を講じて止血し、一群の血液を輸血し、血液凝固因子を含む薬剤を投与します。 播種性血管内凝固症候群の有意な兆候が見られる場合、ヘパリンは10〜000IUのボーラス投与で静脈内投与されます。 腎不全の場合、腹膜血液透析と血漿交換が行われ、良い結果が得られますが、これらの操作を行う前に、ヘパリンの導入は禁忌です。 精神運動の興奮と発作を止めるために、ジプラジン、ハロペリドール、オキシ酪酸ナトリウムが処方されています。 重症の場合は、挿管と機械換気に頼ります。 出血の危険性が高いことを覚えておくことが重要であるため、すべての操作は細心の注意を払って実行する必要があります。 昏睡状態から患者を取り除くとき、次のステップは基礎疾患の集中治療を行うことです。 第9回 衝撃 ショックは、多臓器不全によって現れる身体の臨界状態の一形態であり、一般的な循環の危機に基づいてカスケードで発生し、原則として、治療せずに死に至ります。 ショック要因とは、適応メカニズムを超える身体への影響のことです。 ショックでは、呼吸、心臓血管系、および腎臓の機能が変化し、器官および組織の微小循環のプロセスおよび代謝プロセスが中断されます。 病因と病因 ショックは、多因性疾患です。 発生の病因に応じて、ショックの種類が異なる場合があります。 1. 外傷性ショック: 1)機械的損傷 - 骨折、創傷、軟部組織の圧迫など。 2)火傷(熱傷および化学火傷)を伴う。 3) 低温の影響下 - コールドショック; 4)感電の場合-感電。 2.出血性または血液量減少性ショック: 1)出血、急性失血の結果として発症します。 2)水収支の急激な違反の結果として、体の脱水が起こります。 3.敗血症性(細菌毒性)ショック(グラム陰性菌またはグラム陽性菌の微生物叢によって引き起こされる一般的な化膿性プロセス)。 4.アナフィラキシーショック。 5.心原性ショック(心筋梗塞、急性心不全)。 心臓病学の緊急状態のセクションで考慮されます。 すべてのタイプのショックにおいて、発症の主なメカニズムは血管拡張であり、その結果、血管床の容量が増加し、循環血液量(BCC)が減少します。これは、失血、再分配などのさまざまな要因があるためです。血液と組織の間の液体、または血管容量を増加させる正常な血液量の不一致。 結果として生じる BCC と血管床の容量との不一致は、心拍出量の減少と微小循環障害の根底にあります。 後者は、血液循環の主な機能、つまり細胞と血液の間の物質と酸素の交換がここで行われるため、身体に深刻な変化をもたらします。 血液が濃くなり、粘度が上昇し、毛細血管内の微小血栓症が起こります。 その後、細胞機能は死に至るまで破壊されます。 組織では、嫌気性プロセスが好気性プロセスよりも優勢になり始め、代謝性アシドーシスの発症につながります。 代謝産物、主に乳酸の蓄積は、アシドーシスを増加させます。 敗血症性ショックの病因の特徴は、動静脈シャントの開放に寄与する細菌毒素の影響下での血液循環の侵害であり、血液は毛細血管床を迂回し始め、細動脈から細静脈に流れます。 毛細血管の血流が減少し、細菌毒素が細胞に特異的に作用するため、細胞の栄養が破壊され、細胞への酸素供給が減少します。 アナフィラキシーショックでは、ヒスタミンやその他の生物学的に活性な物質の影響下で、毛細血管と静脈が緊張を失い、末梢血管床が拡張するにつれてその容量が増加し、血液の病理学的再分布につながります。 血液が毛細血管と細静脈に蓄積し始め、心臓の活動に違反します。 同時に形成されるBCCは血管床の容量に対応しておらず、それに応じて心臓の分時換気量(心拍出量)が減少します。 結果として生じる微小循環床での血液の停滞は、毛細血管床のレベルでの細胞と血液との間の代謝および酸素の破壊につながる。 上記のプロセスは、肝臓組織の虚血およびその機能の破壊につながり、ショック発生の重度の段階で低酸素症をさらに悪化させます。 肝臓の解毒、タンパク質形成、グリコーゲン形成およびその他の機能の侵害。 腎組織における主要な局所血流および微小循環の障害は、腎臓の濾過および濃縮機能の両方の破壊に寄与し、乏尿から無尿への利尿の減少をもたらし、患者の体内に窒素性廃棄物が蓄積する.尿素、クレアチニン、およびその他の有毒な代謝産物物質などの体。 副腎皮質の機能が損なわれ、コルチコステロイド(グルココルチコイド、ミネラルコルチコイド、アンドロゲンホルモン)の合成が減少し、進行中のプロセスが悪化します。 肺の循環障害は、外呼吸の侵害、肺胞ガス交換の減少、血液シャントの発生、微小血栓症の形成を説明し、その結果、組織の低酸素症を悪化させる呼吸不全の発症を引き起こします。 診療所 出血性ショックは、結果として生じる失血に対する体の反応です(BCCの25-30%の喪失は、重度のショックにつながります)。 火傷ショックの発生では、痛みの要因と大量の血漿喪失が支配的な役割を果たします。 急速に発達する乏尿と無尿。 ショックの発症とその重症度は、失血の量と速度によって特徴づけられます。 後者に基づいて、代償性出血性ショック、非代償性可逆性ショック、および非代償性不可逆性ショックが区別されます。 代償性ショック、皮膚の蒼白、冷たいべたつきのある汗、脈拍が小さく頻繁になり、血圧は正常範囲内またはわずかに低下しますが、排尿はわずかに減少します。 補償されていない可逆的ショックでは、皮膚と粘膜がシアン化、患者は無気力になり、脈拍は小さく頻繁になり、動脈圧と中心静脈圧が大幅に低下し、乏尿が発生し、アルゴバー指数が増加し、ECGは心筋の酸素供給の違反。 不可逆的なショックの経過により、意識がなくなり、血圧が臨界値まで低下し、検出されない場合があります。皮膚は大理石色で、無尿が発生します-排尿の停止。 アルゴバー指数は高いです。 出血性ショックの重症度を評価するには、出血量であるBCCの測定が非常に重要です。 衝撃強度解析マップと得られた結果の評価を表 4 および表 5 に示します。 表4 衝撃強度分析マップ
表5 総合点による成績評価
ショック指数、またはアルゴバー指数は、収縮期血圧に対する心拍数の比率です。 1度のショックでは、Algover指数は2を超えません。2度では、XNUMX以下です。 指数が XNUMX を超える場合、この状態は生命に適合しないと特徴付けられます。 衝撃の種類 アナフィラキシーショックは、即時型のさまざまなアレルギー反応の複合体であり、極度の重症度に達します。 アナフィラキシーショックには次のような形態があります。 1) 急性循環不全が発生し、しばしば心拍リズム障害、心室および心房細動、および血圧低下を伴う頻脈によって現れる心血管型; 2) 急性呼吸不全を伴う呼吸形態: 息切れ、チアノーゼ、喘鳴、バブリング呼吸、肺の湿ったラ音。 これは、毛細血管循環の違反、肺組織の腫れ、喉頭、喉頭蓋によるものです。 3) 低酸素症、微小循環障害および脳浮腫による脳形態。 コースの重症度に応じて、4度のアナフィラキシーショックが区別されます。 I度(軽度)は、皮膚のかゆみ、発疹の出現、頭痛、めまい、頭の紅潮感が特徴です。 II度(中等度) - クインケ浮腫、頻脈、動脈圧の低下、アルゴバー指数の上昇が以前に示された症状に加わります。 グレードIII(重度)は、意識喪失、急性呼吸器および心血管不全(息切れ、チアノーゼ、喘鳴呼吸、小さな急速な脈拍、血圧の急激な低下、アルゴバー指数の高さ)によって現れます。 IV度(非常に重度)は、意識の喪失、重度の心血管機能不全を伴います:脈拍が決定されず、血圧が低下します。 処理。 治療は、ショック治療の一般原則に従って実行されます:血行動態の回復、毛細血管血流、血管収縮剤の使用、BCCの正常化および微小循環。 具体的な対策は、人体の抗原を不活性化すること(たとえば、抗生物質によって引き起こされるショックにおけるペニシリナーゼまたはβ-ラクタマーゼ)、または抗ヒスタミン薬および膜安定剤などの抗原の身体への影響を防ぐことを目的としています。 1.血行動態が安定するまでアドレナリンの静脈内注入。 ドープミン 10-15 mcg / kg / min を使用でき、気管支痙攣および β-アドレナリン アゴニストの症状がある場合: alupent、brikanil を静脈内に点滴します。 2.反応がこれらの薬剤によって引き起こされない限り、ポリグルシンおよびレオポリグルシンを含む2500〜3000mlの容量での注入療法。 重曹4%400 ml、bccと血行動態を回復するためのブドウ糖溶液。 3.静脈内膜安定剤:プレドニゾロン最大600mg、アスコルビン酸500mg、トロキセバシン5ml、エタムシル酸ナトリウム750mg、シトクロムC 30mg(XNUMX日量が示されている)。 4. 気管支拡張薬: ユーフィリン 240-480 mg、ノシュパ 2 ml、アルペント (ブリカニル) 0,5 mg 点滴。 5.抗ヒスタミン薬:ジフェンヒドラミン40mg(スプラスチン60mg、タベギル6ml)、シメチジン200〜400mgの静脈内投与(XNUMX日量が示されている)。 6.プロテアーゼ阻害剤:トラシロール400万U、収縮性100万U。 外傷性ショックは、重要なシステムや器官の機能が損なわれ、阻害されている、損傷に反応して生じた身体の病理学的かつ重大な状態です。 外傷ショックの間、無気力期と勃起期が区別されます。 発生時までに、ショックは一次(1〜2時間)および二次(損傷後2時間以上)になる可能性があります。 勃起期または発生段階。 意識は残り、患者は青ざめ、落ち着きがなく、多幸感があり、不十分で、悲鳴を上げる、どこかに走る、逃げるなどの可能性があります。この段階では、圧力と脈拍がしばらくの間正常に保たれるため、アドレナリンが放出されます。 このフェーズの期間は、数分から数時間から数日です。 しかし、ほとんどの場合、それは短いです。 患者が無気力で無気力になると、血圧が低下し、頻脈が現れると、勃起期が勃起期に置き換わります。 傷害の重症度の推定値を表6に示します。 表6 傷害の重症度の評価
ポイントを計算した後、結果の数値に係数を掛けます。 注釈 1.怪我の量と重症度のリストに指定されていない怪我がある場合、リストされたもののXNUMXつに対応する重症度に応じて、怪我の種類に応じてポイント数が付与されます。 2.身体の適応機能を低下させる身体疾患がある場合、検出されたポイントの合計に1,2から2,0の係数が掛けられます。 3. 50〜60歳の場合、ポイントの合計は1,2倍になり、それより古い場合は1,5倍になります。 処理。 治療の主な方向性。 1.外傷剤の作用の排除。 2.血液量減少の解消。 3. 低酸素症の解消。 麻酔は、鎮痛剤や薬物の導入、封鎖の実施によって行われます。 酸素療法、必要に応じて、気管挿管。 失血とBCC(血漿、血液、レオポリグルシン、ポリグルシン、赤血球腫)の補償。 代謝の正常化、代謝性アシドーシスが進行するにつれて、塩化カルシウム10%-10 ml、塩化ナトリウム10%-20 ml、ブドウ糖40%-100mlが導入されます。 ビタミン欠乏症(グループBのビタミン、ビタミンC)と戦ってください。 グルココルチコステロイドによるホルモン療法 - プレドニゾロンを静脈内に90回60ml、その後10時間ごとにXNUMXml。 血管緊張の刺激(メザトン、ノルエピネフリン)、循環血液の補充量のみ。 抗ヒスタミン剤(ジフェンヒドラミン、シバゾン)も抗ショック療法に関与しています。 出血性ショックは、大量の失血の後に発症する急性心血管不全の状態であり、重要な臓器の灌流の減少につながります。 病因:大血管の損傷、急性胃および十二指腸潰瘍、大動脈瘤の破裂、出血性膵炎、脾臓または肝臓の破裂、管の破裂または子宮外妊娠、子宮内の胎盤小葉の存在などを伴う損傷。 臨床データと血液量の不足の大きさによると、次の重症度が区別されます。 1.表現されていません-臨床データはありません。血圧のレベルは正常です。 失血量は最大10%(500ml)です。 2.弱い-最小限の頻脈、血圧のわずかな低下、末梢血管収縮の兆候(手足の冷え)。 失血量は 15 ~ 25% (750 ~ 1200 ml) です。 3. 中程度 - 毎分 100 ~ 120 回の頻脈、脈圧の低下、収縮期圧 1 ~ 90 mm Hg。 アート、不安、発汗、蒼白、乏尿。 失血量は 100 ~ 25% (35 ~ 1250 ml) です。 4. 重度 - 毎分 120 回を超える頻脈、収縮期血圧が 60 mm Hg 未満。 アート、眼圧計、昏迷、極度の蒼白、四肢の冷え、無尿によって決定されないことがよくあります。 出血量は35%以上(1750ml以上)。 血液の一般的な分析、ヘモグロビン、赤血球、ヘマトクリットのレベルの低下の実験室。 心電図では、ST セグメントと T 波に非特異的な変化が見られますが、これは冠循環の不足によるものです。 出血性ショックの治療には、止血、BCCを回復させるための注入療法の使用、状況に応じた血管収縮剤または血管拡張剤の使用が含まれます。 輸液療法では、4リットルの液体と電解質(生理食塩水、ブドウ糖、アルブミン、ポリグルシン)を静脈内投与します。 出血の場合、単一群の血液と血漿の輸血は、少なくとも4回分の総量で示されます(1回分は250mlです)。 膜安定剤(プレドニゾロン90~120mg)などのホルモン剤の導入が示されています。 病因に応じて、特定の治療が行われます。 敗血症性ショックは、感染性病原体が最初の病巣から血液系に浸透し、全身に広がることです。 原因物質は、ブドウ球菌、連鎖球菌、肺炎球菌、髄膜炎菌、腸球菌、および大腸菌、サルモネラ菌、緑膿菌などです。敗血症性ショックには、肺、肝臓、腎臓系の機能障害、血液の侵害が伴います。血栓出血症候群につながる凝固系( マチャベリ症候群)、敗血症のすべての症例で発症します。 敗血症の経過は病原体の種類の影響を受けます。これは、現代の治療法では特に重要です。 実験室進行性貧血が認められる(溶血および造血の抑制による)。 ただし、12 109 / lまでの白血球増加症は、造血器官の急激な低下が形成されるため、重篤な場合には白血球減少症も観察されることがあります。 細菌性ショックの臨床症状:悪寒、高熱、低血圧、乾燥した暖かい皮膚-最初は、そして後で-冷たく湿った、蒼白、チアノーゼ、精神状態障害、嘔吐、下痢、乏尿。 好中球増加症を特徴とし、白血球の処方が左から骨髄球にシフトします。 ESRは30〜60 mm/h以上に増加します。 血中ビリルビンのレベルが上昇し(最大35-85 µmol / l)、これは血中の残留窒素の含有量にも当てはまります。 血液凝固とプロトロンビン指数が低下し(最大50-70%)、カルシウムと塩化物の含有量が減少します。 アルブミンが原因で発生する総血中タンパク質が減少し、グロブリン(α-グロブリンおよびb-グロブリン)のレベルが上昇します。 尿中、タンパク尿、白血球、赤血球、円柱。 尿中の塩化物のレベルが低下し、尿素と尿酸が上昇します。 治療は本質的に病因であるため、抗生物質療法を処方する前に、病原体とその抗生物質に対する感受性を判断する必要があります。 抗菌剤は最大用量で使用する必要があります。 敗血症性ショックの治療には、グラム陰性微生物の全スペクトルをカバーする抗生物質を使用する必要があります。 最も合理的なのは、緑膿菌に対して有効であることが証明されているセフタジジムとインピネムの組み合わせです。 クリンダマイシン、メトロニダゾール、チカルシリン、イミピネムなどの薬剤は、耐性病原体が発生した場合に最適な薬剤です。 ブドウ球菌が血液から播種された場合は、ペニシリン群の薬で治療を開始する必要があります。 低血圧の治療は、血管内液量の妥当性における治療の最初の段階にあります。 クリスタロイド溶液(等張塩化ナトリウム溶液、乳酸リンゲル液)またはコロイド(アルブミン、デキストラン、ポリビニルピロリドン)を使用してください。 コロイドの利点は、コロイドが導入されると、必要な充填圧力に最も早く到達し、その圧力が長時間維持されることです。 効果がない場合は、強心剤および(または)血管作用薬が使用されます。 ドーパミンは、心選択的なβ作動薬であるため、最適な薬物です。 コルチコステロイドは、エンドトキシンに対する全体的な反応を低下させ、発熱を抑え、血行動態にプラスの効果をもたらします。 60日90~XNUMXmgのプレドニゾロン。 講義番号10。急性中毒 急性中毒 - 化学的病因の病気。その臨床像は、生命機能の侵害を引き起こし、生命を危険にさらす可能性のある有毒な量の化学物質を人体にXNUMX回摂取することで発症します。 原因と発生場所に応じて、次のタイプの中毒が区別されます。 1.職場での偶発的な中毒(事故)-事故中または有害物質の使用期間中の技術的安全規則に違反した場合の労働災害への暴露。 日常生活の中で-家庭用化学物質の誤ったまたは誤った使用がある場合、医薬品によるセルフメディケーションの場合、それらの過剰摂取または誤った使用、アルコールおよび薬物中毒、有毒な昆虫およびヘビの咬傷; 医療過誤。 2. 意図的な中毒 - 自殺中毒 (真または実証的) および犯罪中毒 (殺害または無力状態にすることを目的とした); 「警察」(公共の秩序を回復するために化学物質や毒物を使用する場合)およびテロ行為の結果を含む中毒との戦い(化学兵器を使用する場合)。 犠牲者の数に応じて、個人、グループ、集団の急性中毒が区別されます。 有毒物質の摂取は、口(組み込み、経口)、気道(吸入)、保護されていない皮膚(経皮)、非経口注射、または直腸、膣、外耳道への注射によって可能です。 急性中毒の臨床経過では、XNUMXつの段階が区別されます:毒性原性と体形成性です。 毒性段階の本質は、体内の活性物質が特定の毒性効果を引き起こす可能性のある用量を持っていることです. 体形成期は、有毒物質の排除または破壊の後に発生し、臓器やシステムの構造的および機能的状態の「痕跡」または残留違反の形で現れます。 急性中毒の診断の一般原則 1. 臨床診断は、以下のデータに基づいています。 1)中毒の物的証拠を発見するための現場の検査。 2) 被害者等の言葉からの既往歴 - 被害者がどの毒物を摂取したか、毒物を摂取した時間、摂取した毒物量、毒物が体内に浸透した経路を知ることができます。 、中毒などの発症に伴う状況; 3)「選択的毒性」の原則に従って、特定の毒性物質または物質群に特徴的な中毒の特定の症状を特定するために、疾患の臨床像を研究する。 2. 実験室毒性診断は、身体の生物学的媒体 (血液、尿など) 中の有毒物質の定性的または定量的測定を目的としています。 3. 病理学的診断は、中毒の特定の死後兆候の検出にあり、法医学の専門家によって実行されます。 1. メチルアルコール中毒 メチルアルコールは、呼吸器系、消化器系、経皮系のすべての経路で吸収されます。 経口摂取した場合のメタノールの致死量は40〜250 mlの範囲ですが、10〜20mlを摂取しても失明を引き起こす可能性があります。 中毒は、1,5〜2,5%のメタノールを含むさまざまなアルコール混合物を摂取した後にも発生します。 吸収後、メタノールは水溶性であるため、すべての組織に分布します。 最大量は腎臓と胃腸管に蓄積し、最小量は脳、筋肉、脂肪組織に蓄積します。 病理解剖学的病変には、脳浮腫と、網膜神経節細胞の最初は炎症性で、後にはジストロフィー性の性質への損傷が含まれます。 場合によっては、神経系の損傷に加えて、肝臓、腎臓、肺、心筋の変性病変が見られます。 臨床画像 メタノールの毒性効果では、XNUMX 段階の作用を区別することができます。 初期段階 (フェーズ I) では、メタノールは分子全体として体に作用し、主に麻薬効果がありますが、エチル アルコールよりも弱い効果があります。 続いて(フェーズII)、酸化生成物の有害な影響が現れます。 臨床像では、期間が区別されます:中毒、潜在的、または相対的な幸福(数時間から1〜2日続く)、中毒の主な症状、および好ましい結果を伴う逆の発達。 重症度に応じて、軽度、中等度(または眼科)および重度(または全身性)が区別されます。 軽度の中毒では、30分から数時間の潜伏期間の後に、急速な疲労、頭痛、吐き気、軽度の中毒の状態が見られます。 エチルアルコールとメチルアルコールを同時に吸収すると、潜伏期間が長くなり、中毒の重症度が低下します。 中程度の中毒の場合、短い潜伏期間の後、患者は頭痛、めまい、腹部の急性痛(主に上腹部)、嘔吐、落ち着きのなさ、せん妄、痙攣を発症します。 最終的に、深い昏睡状態に陥ります。 中枢性の呼吸不全が発生し、続いて心血管不全が起こると、患者は低体温症、場合によってはチアノーゼを発症します。 この段階で、瞳孔は拡張し、眼底の研究は網膜浮腫の存在を示します。 視力の低下、視野の狭小化、瞳孔の拡大、光に対する反射喪失、眼球の痛みなどの特徴的な視覚障害が2日目から6日目に発生します。 眼底を検査すると、視神経萎縮の徴候が明らかになります。 最も深刻な合併症は全盲です。 治療 治療には以下の点が含まれます。 1.体内への毒の侵入を止める。 毒物の使用の中止、汚染された雰囲気からの除去、皮膚からの毒物の除去。 2.非吸収毒の除去(消化管から): 1) プローブ胃洗浄; 2)吸着剤または生理食塩水下剤の使用。 3) クレンジングまたはサイフォン浣腸。 3.吸収された毒の除去: 1) 利尿を強制する; 2)体外解毒の方法(血液吸着、血液透析、腹膜透析、血液置換手術)。 4.解毒剤療法、すなわち、物理的または化学的中和による毒の中和、および適用ポイントをめぐる毒との競争。 6. 体の重要な機能を維持します。 7.体の水電解質、酸塩基状態の正常化。 8. 長期的な結果と合併症の治療。 水または 2% 炭酸水素ナトリウム溶液で胃を洗浄した後、30 ml の水に溶かした 100 g の硫酸マグネシウム (ナトリウム) を摂取します。 コルジアミン 2 ml、1% カフェイン溶液 20 ml を皮下投与します。 昏睡状態では、5日あたり患者の体重5 kgあたり1,5〜2 gのアルコールの割合で、1%グルコース溶液中の400%エチルアルコール溶液を静脈内投与します。 ポリグルシン(レオポリグルシン)50ml、プレドニゾロン100〜400mg、グルコソン - ボカイン混合物(5%ノボカイン溶液25mlを含む2%グルコース溶液80ml)、フロセミド(ラシックス)120〜40mg、40ml 8% - XNUMX IUのインスリンを含むグルコース溶液。 2. エチルアルコール中毒 診療所 有毒な用量を服用する場合 - 動揺、運動失調、昏迷、反射の抑制を伴う昏睡、口からのアルコール臭、顔面紅潮、結膜炎、瞳孔の「遊び」、嘔吐、不随意排尿、頻脈、「かすれた」呼吸、虚脱、吐き気のあるwtの誤嚥の可能性がある嘔吐。 治療 太いプローブによる胃洗浄、続いて生理食塩水の下剤、サイフォン浣腸の導入。 アトロピンの1%溶液0,1ml、コルジアミン2ml、カフェインの1%溶液20ml、崩壊を伴う皮下-メザトンの1%溶液1ml。 咽頭反射がない場合 - 気管挿管および人工呼吸。 Astrup式に従って計算された量の4%重炭酸ナトリウム溶液、インスリン、ビタミンBおよびC、コカルボキシラーゼ、ニコチン酸を含む高張(10および20%)グルコース溶液の同時投与による利尿の強制。 呼吸抑制を伴う-エチミゾールの3%溶液5-1,5ml、アミノフィリンの10%溶液2,4ml、エフェドリンの1%溶液5ml、酸素吸入をゆっくりと静脈内投与する。 誤嚥あり-緊急衛生気管支鏡検査。 非経口抗生物質。 3. エチレングリコール(不凍液)中毒 平均致死量は約 100ml です。 消化管で急速に吸収され、すべての組織に分配され、脳内で最大濃度になります。 主な毒性作用は腎実質で観察され、尿細管上皮の壊死、間質性浮腫、および皮質層の出血性壊死の病巣が発生します。 浮腫は脳に見られます。 診療所 酩酊のクリニックでは、3つの期間が区別されます: 1) 初期 - 最大 12 時間持続し、アルコール中毒のタイプによる CNS 損傷の症状が優勢です。 2) 神経毒性 - CNS 損傷の症状が進行し、呼吸器系および心臓血管系の障害が加わる場合。 3) 腎毒性 - 2 日目から 5 日目まで、中毒の臨床像では腎障害が優勢です。 中毒期間の期間と重症度は、中毒の重症度によって異なります。 軽度の場合、中毒の期間 (10 ~ 15 時間) の後、わずかな倦怠感、頭痛、吐き気が発生します。 意識は清明のままで、腎臓の損傷は見られません。 中程度の重症度の中毒の場合、中毒の症状を背景に、嘔吐、下痢、上腹部の痛み、頭痛が発生します。 3〜5日目に、腎臓障害の症状が現れます。 重度の中毒では、急速に意識を失い、項部硬直、間代性緊張性けいれん、発熱、騒々しい深呼吸、虚脱、肺水腫が起こります。 患者が初日に死亡しない場合、腎不全の症状が2〜3日目から発生します。喉の渇き、背中の痛み、尿量の減少、無尿まで。 肝臓が肥大し、痛みを伴います。 尿毒症で死にます。 治療 水または2%重炭酸ナトリウム溶液による胃洗浄、続いて30mlの水に200gの硫酸マグネシウムを導入する。 エチルアルコールの200%溶液30mlの中に。 3mlの水に5-100gの重曹。 たっぷりドリンク。 筋肉内に1〜2 mlのコーディアミン、1 mlの20%カフェイン溶液。 400%アスコルビン酸溶液5mlとインスリン5単位、グルコソン-ボカイン混合物、ポリグルシン5ml、ヘモデズ8ml、フロセミド400-400g、フロセミド80-120mgを含む60%グルコース溶液100mlを静脈内投与するプレドニゾロン。 4. ジクロロエタン中毒 主な侵入経路は、消化管、気道、皮膚です。 経口投与した場合のヒトの DCE の致死量は 10 ~ 20 ml です。 DCE の毒性作用は、中枢神経系への麻薬作用、肝臓、腎臓、胃腸管への損傷、および心血管系への顕著な影響によるものです。 診療所 臨床像では、主な症状は次のとおりです。中毒性脳症、急性中毒性胃炎および胃腸炎、外呼吸障害、中毒性肝炎、腎機能障害。 服用後最初の数時間で、めまい、運動失調、精神運動興奮、間代性強直性痙攣、意識の低下、昏睡までが現れます。 中毒の初期の兆候のXNUMXつは、吐き気の形の胃腸障害、胆汁の混合による嘔吐の繰り返しです。 外呼吸の機能障害は、閉塞性誤嚥タイプに応じて発生することが多く、唾液分泌の増加、気管支漏出、および誤嚥を伴います。 呼吸中枢の機能の阻害、呼吸筋の緊張亢進の発生、および胸部の硬直が認められます。 重度の合併症は、皮膚の冷却およびチアノーゼ、冷汗、息切れ、頻脈および循環血液量減少によって現れる外毒性ショックです。 腎臓の排泄機能の低下。 DCE中毒の重症度に応じて、次のように分類されます。 1.軽度の中毒、消化不良障害、軽度の神経症状、軽度の肝障害の発症を特徴とします。 2.中程度の中毒。 中毒性胃炎、胃腸炎、中毒性脳症、中等度の肝障害、軽度の腎症の症状を伴う。 3.中毒性脳症、重度の肝障害、中毒性腎症、胃腸炎の重篤な症状を伴う重度の中毒が発生します。 蒸気中毒、頭痛、眠気、口の中の甘い味、口からの毒のにおい、粘膜の刺激感、意識の喪失、強膜と皮膚の黄色化を伴う急性肝腎不全、肝臓の肥大の場合、無尿が発生します。 摂取すると、嘔吐、腹痛、毒の匂いを伴う軟便、強膜の充血、精神運動性興奮、うつ病と昏睡、虚脱、中毒性ショック、出血性症候群、急性肝腎不全が繰り返されます。 毒が皮膚につくと、皮膚炎が発症します。 治療 蒸気による中毒の場合 - 呼吸抑制IVLを伴う患部からの犠牲者の除去。 毒が内部に入った場合 - 厚いプローブを介した胃洗浄、続いて3mlの水と4〜200mlのワセリン油、サイフォン浣腸に大さじ150〜200杯の粉末活性炭を導入します。 チオ硫酸ナトリウムの20%溶液40〜30 mlを静脈内投与し、ユニトリオールの5%溶液5mlを筋肉内投与します。 静脈内に400mlのポリグルシン、400mlのヘモデズ、400mlの5%グルコース溶液、80-120mgのフロセミド(ラシックス)、6-8mlのアスコルビン酸の5%溶液。 筋肉内に2mlのコルジアミン、崩壊あり-1mlのメザトン1%溶液、1mlの20%カフェイン溶液、100-150mgのプレドニゾロン。 肝腎不全の増加に伴い、特定の治療法が実施されます。 ポリグルシン 400 ml、ゲモデス 400 ml、400% グルコース 5 ml、フロセミド 80 ~ 120 mg、6% アスコルビン酸 8 ~ 5 ml、プレドニゾロン 100 ~ 150 mg、1 % 1 ml の静脈内ボーラスメザトン。 2% チアミン臭化物 4 ~ 6 ml および 2% ピリドキシン 4 ~ 5 ml を筋肉内投与。 精神運動的興奮を伴い、フェノゼパムの1%溶液3ml。 呼吸抑制を伴う酸素吸入 - 呼吸チューブを介した IVL。 初日の最も効果的で控えめな方法は腹膜透析です。 標準的な透析液の組成には、塩化カリウム0,3 g、塩化ナトリウム8,3 g、塩化マグネシウム0,1 g、塩化カルシウム0,3 g、水6リットルあたりのグルコース1gが含まれます。 同時に、2万単位のペニシリンと500単位のヘパリンを加えた最大1000リットルの電解質溶液が患者の腹腔に注入されます。 中毒の体形成期では、主な治療法は、肺炎、肝障害などの発症した合併症の治療を目的としています。 5.有毒キノコ中毒(ベニテングタケ、偽キノコ、アミガサタケ、カイツブリ) 診療所 1~2時間から36時間の潜伏期間の後、痙攣性の腹痛、流涎、吐き気、不屈の嘔吐、下痢、脱水、虚脱、せん妄、幻覚、痙攣が現れる。 2〜3日目 - 無尿、高窒素血症、黄疸を伴う腎不全および肝不全の現象。 ラインやモレルによる重度の中毒では、溶血が起こる可能性があります。 治療 太いプローブによる胃洗浄、続いて水 3 ml 中の粉末活性炭大さじ 4 ~ 200 および水 30 ml 中の硫酸マグネシウム (ナトリウム) 100 g の導入、サイフォン浣腸。 アトロピンの1%溶液0,1ml、コージアミン2mlを皮下投与。 アミガサタケ中毒では、アトロピンは解毒剤として使用されていません。 ポリグルシン400ml、ゲモデス400ml、400%アスコルビン酸溶液5〜4mlを含む6%グルコース溶液5ml、フロセミド(ラシックス)80〜120mgを静脈内投与する。 チアミン臭化物の 1% 溶液 2 ~ 6ml とピリドキシン塩酸塩の 2% 溶液 5ml を筋肉内注射します (注射器 XNUMX 本で注射しないでください)。 プラチフィリンの1%溶液0,2ml、パパベリンの2%溶液2mlの導入による筋肉内疼痛症候群の緩和。 けいれん、精神運動興奮 - フェノゼパムの1%溶液2〜3mlまたは溶解混合物(クロルプロマジンの1%溶液2〜2,5ml、ジメドロールの1%溶液2〜1ml、5〜10 ml 25% 硫酸マグネシウム溶液) 血圧の制御下で。 強制利尿。重症の場合 - 血液吸収、早期の血液透析。ヒモやアミガサタケによる重度の中毒の場合、重度の溶血の場合、血液透析の可能性がない場合は、血液置換手術が行われます。 Astrup 式に従って決定された量の重炭酸ナトリウムの 4% 溶液を静脈内投与することによるアシドーシスの矯正。抗生物質 - ベンジルペニシリン 10 日あたり最大 XNUMX 万単位。 対症療法。 肝不全および腎不全の増加に伴い、インスリン、グループBおよびCのビタミン、5〜10 IUのヘパリン、アミノフィリンを含む20〜30%のグルコース溶液による注入療法。 6.ヘビ毒中毒 診療所 咬傷部位の痛みと急速に広がる腫れ、眠気、呼吸抑制、虚脱、ヘモグロビン尿を伴う血管内溶血、重度の皮下出血、時には痙攣。 おそらく腎不全。 コブラの咬傷では、局所的な変化はそれほど顕著ではなく、球の障害(発話および嚥下障害、眼瞼下垂、運動筋の麻痺)および呼吸抑制が優勢です。 水平位置での完全な休息を示します。 傷口から最初の一滴の血を絞り出します。 負傷した手足の固定。 一口の代わりに - 寒い。 豊富なドリンク。 治療 吸血ジャーを使用して、咬傷部位に形成された創傷からの血液とリンパ液の吸引(咬傷後30〜60分以内)。 1%過マンガン酸カリウム溶液で創傷を洗浄します。 創傷への導入アドレナリンの0,3%溶液0,5-0,1ml。 可能であれば、100〜150 mlのヒドロコルチゾンまたは50〜100 mlのプレドニゾロンを予備的に静脈内注射した後、特定の一価または多価の抗ヘビ血清を緊急に導入します。 コブラ咬傷の場合-プロゼリンの300%溶液1mlと組み合わせた0,05mlの用量の静脈内アンチコブラ血清およびアトロピンの30%溶液1mlを0,1分ごとに繰り返し投与する。 予防的-ベズレドカによる抗破傷風血清、静脈内分極混合物、10万〜15単位のヘパリン、1〜2mlの1%ジフェンヒドラミン溶液、10mlの10%塩化カルシウム(グルコン酸塩)溶液、5〜10mlの5 %-アスコルビン酸溶液、50-100mgのプレドニゾロンまたは100-150mgのヒドロコルチゾン、400mlのゲモデズ、400mlのポリグルシン、40-80mgのラシックス。 プロメドールの1%溶液2mlの静脈内投与による鎮痛。 急性呼吸不全 - 呼吸管による機械的換気、酸素吸入。 重度の中毒症 - 肝腎不全の進行を伴う血液吸着 - 血液吸着と組み合わせた血液透析。 対症療法。 7.濃酸(硝酸、酢酸、硫酸)による中毒 診療所 蒸気を吸入すると、目や上気道が刺激されます (流涙、鼻水、咳、息切れ)。 反射性呼吸停止の可能性があります。 潜伏期間(2〜24時間)の後、中毒性肺炎または中毒性肺水腫が形成されます。 目に当たった場合、皮膚に当たった場合 - 化学火傷。 摂取すると、口腔、咽頭、食道、胃の化学火傷、呼吸不全を伴う喉頭の腫れの可能性があります。 血を伴う嘔吐、腹膜の炎症、食道や胃の穿孔を繰り返す。 虚脱、ショック、出血症候群。 可能性のある血管内溶血、ヘモグロビン尿性ネフローゼ、急性腎(腎肝)機能不全。 チューブレス胃洗浄と人工嘔吐は、食道の再燃や酸吸引の可能性があるため危険です。 生理食塩水の下剤やアルカリ溶液を注射しないでください。 治療 プロメドールの1%溶液2〜2 mlを予備的に静脈内または筋肉内注射した後、太いチューブから冷水で胃洗浄を行います。 氷の中に、アルマゲルA 15〜20mlを毎時。 静脈内に800mlのポリグルシン、400mlのヘパリン、グルコソン-ボカイン混合物(400mlの5%グルコース溶液と25mlの2%ノボカイン溶液)、50-150mgのプレドニゾロンまたは150-250mgのヒドロコルチゾン、10万単位ヘパリンの、80-120mgのフロセミド(Lasix)。 疼痛症候群の軽減は、フェンタニルの1%溶液2〜0,005mlとドロペリドールの2%溶液4〜0,25mlを静脈内に導入することで達成され、腹部に持続的な痛みがあります-筋肉内に1〜2mlのplatyfillin の 0,2% 溶液、2% パパベリン溶液 2 ml。 消泡剤による酸素の吸入。 喉頭浮腫の増加に伴い、プレドニゾロン200〜400 mg、ジフェンヒドラミン1%溶液2〜1 ml、アミノフィリン10%溶液20〜2,4 ml、エフェドリン1%溶液2〜5mlを静脈内投与します。 効果がない場合-気管切開、適応症による酸素吸入-機械的人工呼吸。 8. ヒ素およびその化合物による中毒 診療所 口の中が金属味、腹痛、嘔吐、軟便、重度の脱水、痙攣、頻脈、血圧低下、昏睡、急性腎不全。 ヒ素水素中毒は、血管内溶血、ヘモグロビン尿症を発症します。 治療 厚いプローブを介した胃洗浄(2日3〜50回)の開始時と終了時にユニチオールの5%溶液5mlを導入し、ユニチオールを加えてサイフォン浣腸を繰り返します。 ユニチオールの300%溶液(20日あたり最大10 ml)の導入による静脈内または筋肉内の解毒療法の継続、1%グルコース溶液400 ml中の5%テタシンカルシウム(EDXNUMXA)XNUMX mlの点滴。 ヒ素水素による中毒の場合-筋肉内に、メカプチドの1%溶液2〜40ml(6日あたり最大8〜XNUMXml)。 高張(10〜20%グルコース溶液)ポリイオン溶液、Astrup式に従って計算された容量の4%重炭酸ナトリウム溶液、グルコソン - ボカイン混合物、アミノフィリン、ビタミンBおよびC、シトクロムCの同時投与による利尿の強制。 重度の中毒 - 早期血液透析。 血液透析を行う過程で、5%ユニチオール溶液が静脈内注射されます(重度の中毒の場合は30〜40 ml / h、中等度の中毒の場合は20〜30 ml / h)。 急性溶血および血液透析不能の場合には、血液置換手術が行われる。 9.灰汁中毒 診療所 摂取すると、口腔、食道、および胃の粘膜の化学火傷が発生します。 食道と腹部に沿った痛み、血液の混じった嘔吐、食道胃出血。 食道、縦隔炎、腹膜炎の発症を伴う胃の穿孔の可能性。 喉頭の火傷 - 声の嗄声、失声、呼吸困難(喘鳴)。 重度の場合 - 火傷、乏尿。 皮膚に接触すると、化学熱傷を引き起こします。 治療 酸中毒と同様に扱う。 10.アトロピン中毒 診療所 口渇、嗄声、乾燥、皮膚充血、瞳孔散大、息切れ、動悸、頻脈、喉の渇き、吐き気、排尿困難。 重度の中毒 - 精神運動興奮、せん妄、幻覚、痙攣、心拍リズム障害、昏睡、虚脱の可能性があります。 治療 必要に応じて-ワセリンオイルで十分に潤滑された厚いプローブによる胃洗浄、大さじ3〜4杯の導入。 l。 200mlの水に粉末活性炭を入れ、30mlの水に100mgの硫酸マグネシウムを入れます。 静脈内に2-4mlの0,05%プロセリン溶液、400-800mlの5%グルコース溶液、40-80mgのフロセミド(ラシックス)。 たっぷりドリンク。 フェノゼパムの1%溶液または溶解混合物(アミナジンの2%溶液3ml、ジフェンヒドラミンの2%溶液2,5mlおよび2ml硫酸マグネシウムの1%溶液)または10-25mlの水あたり1〜2gのデンプンを含む抱水クロラール中の1〜2gの抱水クロラール、静脈内に25〜50mlの10%ヒドロキシ酪酸ナトリウム溶液、15〜20セデュクセンの2%溶液のml。 重度の頻脈、期外収縮 - 静脈内アナプリリン(1%溶液2〜0,25 ml)または舌の下のアナプリリン錠剤(40 mg)。 崩壊を伴う - 塩化ナトリウムの1%溶液1ml中のメザトンの10%溶液0,9mlを静脈内投与。 鋭い高体温で - 筋肉内に2mlの50%鎮痛剤溶液、大きな血管と頭のアイスパック、ウェットラップ。 11.麻中毒(ハシシ、マリファナ、マリファナ、計画) 診療所 多幸感、精神運動性興奮、鮮明な視覚的幻覚、散大した瞳孔、耳鳴りがあります。 その後、衰弱、無気力、気分の落ち込み、眠気、徐脈、低体温。 治療 経口中毒の場合-厚いプローブによる胃洗浄、続いて3mlの水に4-200杯の粉末活性炭を導入します。 アスコルビン酸の400%溶液800-5mlとインスリン5-10単位、フロセミド(ラシックス)5-8mg、16%溶液40mlを含む80%ブドウ糖溶液2-6mlを静脈内投与チアミン臭化物の。 鋭い興奮で-筋肉内にクロルプロマジンの3%溶液または溶解混合物の5-2,5ml(クロルプロマジンの2%溶液の2,5ml、ジフェンヒドラミンの1%溶液の2-1mlおよび5の10-25ml %-血圧の制御下にある硫酸マグネシウムの溶液)。 酸素吸入。 利尿を強制する。 重症の場合、血液吸着に頼ります。 12.コカインとジカイン中毒 診療所 一般的な動揺、頭痛、顔面紅潮、瞳孔の拡張、頻脈、呼吸の増加、血圧の上昇、幻覚によって臨床的に現れます。 重症の場合-けいれん、昏睡、呼吸麻痺、虚脱。 治療 過マンガン酸カリウムの 0,1% 溶液を用いた濃厚プローブによる胃洗浄を繰り返した後、大さじ 3 ~ 4 杯を導入します。 l. 200mlの水に粉末活性炭、30mlの水に100gの硫酸マグネシウム。 ゲモデス400ml、400%アスコルビン酸溶液5〜5mlを含む10%グルコース溶液5ml、フロセミド(ラシックス)40〜80mgを静脈内投与する。 興奮した場合 - 犠牲者を固定し、筋肉内にフェノゼパムの1%溶液2〜3 mlまたは溶解混合物(クロルプロマジンの1%溶液2〜2,5 ml、ジフェンヒドラミンの2%溶液1 mlおよび5〜10 ml血圧の制御下での25% - 硫酸マグネシウムの溶液)。 痙攣を伴う場合、抱水クロラール1〜2 gを浣腸に入れ、1〜2 mlの水に25〜50 gのデンプンを加え、効果がない場合は15〜20 mlの20%オキシ酪酸ナトリウム溶液をゆっくりと静脈内投与します。チオペンタールナトリウムまたは浣腸液の20%溶液2,5mlまでゆっくりと筋肉内投与します。 昏睡状態の発症に伴い - 頭にアイスパック、アスコルビン酸の40%溶液40〜4mlおよびインスリン6単位を含む5%グルコース溶液8mlを静脈内にゆっくりとまたは筋肉内に2〜4ml臭化チアミンの6%溶液およびピリドキシン塩酸塩の5%溶液2~4ml、フロセミド80~120mg。 重度の呼吸抑制がある場合は、機械的人工呼吸を行い、ゆっくりと2 mlのコージアミンを静脈内投与し、酸素を吸入します。 13.麻薬性鎮痛薬(モルヒネ、オムノポン、ドロペリドール)による中毒 診療所 眠気または意識喪失、瞳孔収縮、筋緊張亢進(時には痙攣)、呼吸抑制、徐脈、虚脱。 呼吸麻痺は、患者の意識を維持したままで可能です。 治療 (意識を維持しながら)厚いプローブを介した胃洗浄、続いて大さじ3〜4杯の粉末活性炭と30 gの硫酸ナトリウム、サイフォン浣腸の導入。 400mlのgemodez、400mlのポリグルシン、400mlの5%グルコース溶液、60〜80mgのフロセミド(lasix)を静脈内投与。 アトロピンの 1% 溶液 2 ~ 0,1 ml、コルジアミン 1 ~ 2 ml、カフェインの 1% 溶液 20 ml を皮下投与します。 昏睡状態、頭部の保冷剤、アスコルビン酸の40%溶液40〜5mlおよびインスリン10単位を含む5%グルコース溶液8mlの静脈内投与、静脈内ゆっくりまたは筋肉内2〜4ml臭化チアミンの6%溶液およびピリドキシン塩酸塩の5%溶液2~4ml、フロセミド(ラシックス)80~120mg。 必要に応じて、膀胱カテーテル法と尿抽出。 呼吸抑制を伴う - IVL、酸素吸入。 吸血(意識が回復するまで2日3~XNUMX回)。 第11回 痛みと鎮痛薬 1.痛み 痛みは、組織に対する実際のまたは潜在的な病理学的影響による不快な感覚および感情状態です。 CNSでは、痛みはXNUMXつの主要な経路に沿って行われます。 特定の経路 - 脊髄の後角、視床の特定の核、後中心回の皮質。 この経路は、低ニューロンであり、高速で、閾値を伝導し、感情的に色付けされておらず、正確に局所化された痛み (epicritic な痛み) です。 非特異的な方法 - 脊髄の後角、視床の非特異的な核、前頭葉および頭頂葉の皮質がびまん性に。 サブスレッショルド、感情的に色付けされた、不十分に局所化された痛みを引き起こします。 それは、延髄、網状体、大脳辺縁系、および海馬への多数の側副路を形成するため、ゆっくりと多神経性です。 サブスレッショルドの痛みの衝動は、視床で加算されます。 非特異的な痛みの経路に沿って伝導される衝動は、大脳辺縁系の感情中枢、視床下部の自律神経中枢、および延髄を興奮させます。 したがって、痛みには恐怖、痛みを伴う経験、呼吸の増加、脈拍、血圧の上昇、瞳孔の拡張、消化不良が伴います。 侵害受容性疼痛系の作用は、抗侵害受容系によって打ち消され、その主なニューロンは中脳水道周囲灰白質に局在します (シルビウス水道は III 脳室と IV 脳室を接続します)。 それらの軸索は、延髄および脊髄への下降経路と、網様体、視床、視床下部、辺縁系、大脳基底核、および皮質への上昇経路を形成します。 これらのニューロンのメディエーターは、ペンタペプチド: メテンケファリンとロイエンケファリンであり、末端アミノ酸としてそれぞれメチオニンとロイシンを持っています。 エンケファリンはアヘン受容体を興奮させます。 エンケファリン作動性シナプスでは、オピエート受容体はシナプス後膜に位置していますが、同じ膜は他のシナプスのシナプス前です。 オピエート受容体はアデニル酸シクラーゼに関連しており、ニューロンの cAMP 合成を阻害することでその阻害を引き起こします。 その結果、疼痛メディエーターを含むメディエーターのカルシウムの侵入と放出 - ペプチドが減少します:サブスタンスP、コレシストキニン、ソマトスタチン、グルタミン酸。 オピエート受容体は、メディエーターであるエンケファリンだけでなく、抗侵害受容システムの他の成分である脳ホルモン(エンドルフィン)によっても興奮します。 オピエート受容体のペプチドアゴニストは、脳のペプチド物質であるプロオピオコルチン、プロエンケファリンAおよびBのタンパク質分解中に形成されます。これらのペプチドはすべて視床下部で形成されます。 オピエート受容体は、痛みの伝導と知覚、痛みに対する感情的に色付けされた反応の形成に関与するすべての脳構造の受容体を興奮させます。 同時に、痛みのメディエーターの放出が減少し、痛みに伴うすべての反応が弱まります。 2. 鎮痛薬 鎮痛剤(アセチルサリチル酸、パラセタモール、モルヒネ)は、さまざまな原因の痛みを軽減する薬です。 制酸薬、エルゴタミン(片頭痛)、カルバマゼピン(神経痛)、ニトログリセリン(狭心症)など、特定の原因因子によってのみ引き起こされる痛みを軽減する薬、または特定の痛み症候群を解消する薬は、古典的な鎮痛薬には属しません。 コルチコステロイドは、炎症反応とその結果生じる痛みを抑制しますが、これらの目的で広く使用されているにもかかわらず、古典的な鎮痛薬ではありません. 鎮痛薬は、中枢神経系の構造に作用して眠気を引き起こすオピオイドなどの麻薬性と、主に末梢構造に作用するパラセタモール、アセチルサリチル酸などの非麻薬性に分類されます。 鎮痛剤の効果を高める追加の薬 このグループの薬はそれ自体鎮痛薬ではありませんが、痛みに対する態度、その知覚、不安、恐怖、うつ病のレベルを変えることができるため、痛みに対して鎮痛薬と組み合わせて使用 されます(三環系抗うつ薬は、終末期の患者ではモルヒネ)。 このような薬は、向精神薬のほか、平滑筋や横紋筋のけいれんを解消するなど、痛みのメカニズムに影響を与える薬でもかまいません。 麻薬性鎮痛薬は、痛みの知覚を選択的に減らし、痛みの感情的な色とそれに伴う栄養を減らすことで痛みへの耐性を高め、多幸感と薬物依存を引き起こす薬草および合成薬です。 麻薬性鎮痛薬は、中枢神経系の境界内でのみ痛みの伝導と知覚を低下させ、主に非特異的経路を抑制します。 このグループの手段は、アヘン受容体を刺激し、抗受容体システムのペプチドの効果と同様の作用を生み出します。 したがって、麻酔の主なメカニズムは次のとおりです。体が脊髄神経節にあるニューロンIの軸索から、後角のゼラチン状物質にあるニューロンIIへの痛みの衝動の伝導の障害脊髄。 視床における閾値下インパルスの総和の抑制。 延髄、視床下部、大脳辺縁系の痛み反応への参加の減少(痛みに対する非強調的な態度)。 麻薬性鎮痛薬とその拮抗薬の分類 分類は以下のとおりです。 1. ピペリジン-フェナントレン誘導体: 1)モルヒネ; 2)コデイン(メチルモルヒネ、鎮痛剤としてモルヒネより5〜7倍弱い); 3)エチルモルヒネ(ジオニン、モルヒネと強度が等しい)。 2.フェニルピペリジン誘導体: 1) プロメドール (モルヒネよりも 3 ~ 4 倍弱い); 2) フェンタニル (モルヒネの 100 ~ 400 倍強力)。 3. ジフェニルメタンの誘導体: 1)ピリトラミド(ジピドロール) - モルヒネと同等。 2) トラマドール (tramal) - モルヒネよりやや劣る。 4. アゴニスト - アンタゴニスト: 1) オピエート受容体アゴニストおよびアヘン受容体アンタゴニスト - ブプレノルフィン (ノルフィン) (モルヒネよりも 25 ~ 30 倍強い); 2) オピエート受容体アゴニストおよびアヘン受容体アンタゴニスト - ペンタゾシン (lexir) (モルヒネより 2 ~ 3 倍弱い) およびブトルファノール (モラドール) (モルヒネと同等)。 アゴニスト-アンタゴニストは、完全なアゴニストよりも多幸感や薬物依存を引き起こす可能性がはるかに低く、弱いです。 ナロフィン - 単独で(例えば、バルビツレート中毒の場合)、軽度のモルヒネ中毒の場合、鎮痛効果があり、縮瞳、徐脈を引き起こし、呼吸中枢の低下を悪化させます。 モルヒネや他のアゴニストによる重度の中毒では、呼吸中枢のオピエート受容体からそれらを排除し、呼吸を回復させます。 不快感、過敏症、うつ病、視線の集中障害を引き起こします。 完全なオピオイド受容体拮抗薬 ナロキソンには独立した作用はなく、麻薬性鎮痛薬による中毒の解毒剤として効果的です。 麻薬性鎮痛薬は、急性の痛みに短時間だけ使用する必要があります。 ほとんどの場合、怪我、火傷、心筋梗塞、腹膜炎に使用されます(診断を明確にし、手術を決定した後)。 麻薬性鎮痛薬は、麻酔を増強するための溶解混合物の一部です。 このグループの薬は、M-抗コリン作動薬および筋萎縮性鎮痙薬と組み合わせて術後の痛みに使用されます。 それらは、肝臓(ペンタゾシン)および腎臓(プロメドール)疝痛を止めるために処方されています。 慢性疼痛は、進行型の悪性腫瘍(ディピドロール、トラマドール、アゴニスト - アンタゴニスト)を除いて、薬を処方するための禁忌です。 麻薬性鎮痛薬は、特殊な種類の麻酔のために向精神薬と組み合わされます。 神経弛緩痛は、フェンタニル (強い、30 ~ 40 分間続く) とドロペリドール (軽度の抗精神病薬) の組み合わせによる鎮痛です。 ドロペリドールには穏やかな鎮静効果があり、感情的な反応を止め、骨格筋の緊張を和らげます。 また、ドロペリドールの重要な効果は制吐と抗ショックです。 ドロペリドールの投与量 - 1:50。併用薬 - タラモナール。 ニューロレプタナルゲシアは、低外傷性手術、脳神経外科の分野、および心筋梗塞などの心臓病学で使用されます。アタルゲシアまたはトランキライザー鎮痛 - シバゾン、フェナゼパムなどの強力なトランキライザーと組み合わせたフェンタニル。 主な欠点は、フェンタニルの強い呼吸抑制と意識の維持です。 講義番号12.麻酔。 麻酔の種類と段階 全身麻酔、または麻酔は、麻薬性鎮痛薬の作用によって引き起こされる、人の意識、痛みの感受性と反射の一時的なシャットダウン、および骨格筋の筋肉の弛緩を特徴とする身体の状態です。中枢神経系。 体内への麻薬物質の投与経路に応じて、吸入麻酔と非吸入麻酔が区別されます。 1.麻酔の理論 現在、麻酔薬の麻薬作用メカニズムを明確に定義する麻酔理論はありません。 利用可能な麻酔理論の中で、最も重要なものは次のとおりです。 薬物は、すべての臓器やシステムに特定の変化を引き起こす可能性があります。 体が麻薬性鎮痛剤で飽和している期間中、患者の意識、呼吸、血液循環の変化に一定の段階があります。 したがって、麻酔の深さを特徴付ける段階があります。 これらの段階は、エーテル麻酔中に特に明確に現れます。 次の 4 つの段階があります。 1) 鎮痛; 2)興奮; 3) 手術段階、4 つのレベルに細分されます。 4) 覚醒の段階。 鎮痛の段階 患者は意識がありますが、いくらかの無気力が見られ、居眠りをしており、単音節で質問に答えています。 表面的な感受性と痛みの感受性はありませんが、触覚と熱に対する感受性は保たれています。 この段階では、痰の切開、膿瘍、診断研究などの短期間の外科的介入が行われます。この段階は短期間で、3〜4分続きます。 興奮段階 この段階では、大脳皮質の中枢は抑制されており、このときの皮質下中枢は興奮状態にあります。 同時に、患者の意識は完全になくなり、顕著な運動と発話の興奮が見られます。 患者は悲鳴を上げ始め、手術台から起き上がろうとします。 皮膚の充血が認められ、脈拍が頻繁になり、収縮期血圧が上昇します。 瞳孔は広くなりますが、光に対する反応は持続し、流涙が見られます。 多くの場合、咳、気管支分泌の増加、時には嘔吐があります。 興奮を背景に外科的介入を行うことはできません。 この期間中、麻酔を強化するために麻薬で体を飽和させ続ける必要があります。 ステージの期間は、患者の全身状態と麻酔科医の経験によって異なります。 通常、励起の持続時間は 7 ~ 15 分です。 外科的段階 この段階の麻酔が始まると、患者は落ち着き、呼吸が落ち着き、心拍数と血圧が正常に近づきます。 この期間中、外科的介入が可能です。 麻酔の深さに応じて、麻酔の 4 つのレベルとステージ III が区別されます。 第 XNUMX レベル: 患者は落ち着いており、呼吸数、心拍数、血圧が初期値に近づいています。 瞳孔は徐々に狭くなり始め、光に対する反応は維持されます。 眼球の滑らかな動き、偏心した配置があります。 角膜反射と咽頭喉頭反射は保たれていました。 筋緊張は維持されるため、このレベルでの腹部手術は行われません。 第 XNUMX レベル: 眼球の動きが停止し、中央の位置に固定されます。 瞳孔が散大し、光に対する反応が弱まります。 角膜反射と咽頭 - 喉頭反射の活動は弱まり始め、第 XNUMX レベルの終わりに向かって徐々に消失します。 呼吸の動きは穏やかで均一です。 動脈圧と脈拍の値は正常値を取得します。 筋緊張が低下し、開腹手術が可能になります。 麻酔は、原則として、第XNUMXレベルと第XNUMXレベルの期間に行われます。 XNUMX 番目のレベルは、深い麻酔として特徴付けられます。 同時に、強い光刺激に反応して瞳孔が拡張します。 角膜反射はありません。 肋間筋を含む骨格筋の完全な弛緩が発達します。 後者により、呼吸運動は表面的または横隔膜になります。 下顎がたるみ、その筋肉が弛緩すると、舌根が沈み込み、喉頭の入り口が閉じます。 上記のすべてが呼吸停止につながります。 この合併症を防ぐために、下顎を前に出し、この位置に保持します。 このレベルでは、頻脈が発生し、脈拍が小さくなり、緊張します。 動脈圧のレベルが低下します。 このレベルで麻酔を行うことは、患者の生命にとって危険です。 第 XNUMX レベル; 光に対する反応がない状態で瞳孔が最大に拡大すると、角膜はくすんで乾燥します。 肋間筋の麻痺が進行すると、呼吸は表面的になり、横隔膜の動きによって行われます。 頻脈が特徴的ですが、脈拍は糸状になり、頻繁になり、末梢では判断が難しくなり、血圧は急激に低下するか、まったく検出されません。 第 XNUMX レベルでの麻酔は、呼吸停止および循環停止が発生する可能性があるため、患者にとって生命を脅かすものです。 覚醒ステージ 麻薬の導入が止まるとすぐに、血中濃度が低下し、患者は麻酔のすべての段階を逆の順序で通過し、覚醒が起こります。 2. 患者の麻酔の準備 麻酔科医は、患者に麻酔と手術の準備をさせる直接的かつしばしば主要な役割を担います。 義務的な瞬間は手術前の患者の検査ですが、同時に、手術が行われる基礎疾患だけでなく、麻酔科医が詳細に尋ねる付随疾患の存在も重要です. 患者がこれらの疾患に対してどのように治療されたか、治療の効果、治療期間、アレルギー反応の存在、最後の悪化の時期を知る必要があります。 患者が計画的に外科的介入を受ける場合、必要に応じて、既存の付随疾患の修正が行われます。 口腔の衛生は、虫歯が存在する場合に重要です。これらの歯は、追加の望ましくない感染源になる可能性があるためです。 麻酔科医は、患者の精神神経学的状態を見つけて評価します。 たとえば、統合失調症では、幻覚剤(ケタミン)の使用は禁忌です。 精神病の期間中の手術は禁忌です。 神経学的欠損がある場合、それは予備的に修正されます。 アレルギー歴は麻酔科医にとって非常に重要です, このため, 薬への不耐性, 食物, 家庭用化学物質などが指定されています. 患者が悪化したアレルギー既往歴を持っている場合, 薬にさえ, 麻酔中, アレルギー反応アナフィラキシーショックまで発症する可能性があります。 したがって、脱感作剤(ジフェンヒドラミン、スプラスチン)が大量に前投薬に導入されます。 重要なポイントは、過去の手術と麻酔における患者の存在です。 麻酔が何であったか、合併症があったかどうかがわかります。 顔の形、胸の形と種類、首の構造と長さ、皮下脂肪の重症度、浮腫の存在など、患者の身体的状態に注意が払われます。 これはすべて、麻酔と薬の正しい方法を選択するために必要です。 手術中および麻酔を使用するときに患者を麻酔に備えるための最初の規則は、胃腸管の洗浄です(胃はチューブを通して洗浄され、洗浄浣腸が行われます)。 心理的感情的反応を抑制し、迷走神経の活動を抑制するために、手術前に患者に投薬-前投薬が行われます。 夜間は、フェナゼパムが筋肉内に処方されます。 神経系が不安定な患者には、手術の前日に精神安定剤(seduxen、relanium)が処方されます。 手術の40分前に、麻薬性鎮痛薬を筋肉内または皮下に投与します:プロモロールの1〜1%溶液2mlまたはペントゾシン(レキシル)1ml、フェンタニル2ml、または1%モルヒネ1ml。 迷走神経の機能を抑制し、唾液分泌を減少させるために、アトロピンの0,5%溶液0,1mlを投与します。 手術の直前に、除去可能な歯と除去された補綴物の存在について口腔が検査されます。 3.静脈麻酔 静脈内全身麻酔の利点は、患者を麻酔に迅速に導入できることです。 このタイプの麻酔では、興奮がなく、患者はすぐに眠りに落ちます。 しかし、静脈内投与に使用される麻薬は短期間の麻酔を引き起こすため、純粋な形で長期手術の単麻酔薬として使用することはできません. バルビツール酸塩 - ナトリウムチオペンタールとヘキセナール - は、興奮の段階がなく、目覚めが速い間、麻薬睡眠を素早く誘発することができます. チオペンタールナトリウムとヘキセナールによる麻酔の臨床像は似ています。 ゲクセナールは、呼吸中枢に対する抑制効果が少ないです。 バルビツール酸誘導体の新たに調製された溶液が使用される。 バイアルの内容物(薬物1g)を、麻酔開始前に100mlの等張塩化ナトリウム溶液(1%溶液)に溶解する。 末梢静脈または中心静脈(適応症による)に穴を開け、調製した溶液を 1 ml の速度で 100 ~ 1 秒間ゆっくりと注入します。 溶液を 1 ~ 10 ml の量で注入すると、バルビツール酸誘導体に対する患者の感受性が 15 秒以内に測定されます。 アレルギー反応が見られない場合は、麻酔の外科的段階まで薬の導入を続けてください。 麻薬性睡眠の開始以来、麻酔薬の単回注射で、麻酔の持続時間は10〜15分です。 麻酔を維持するために、バルビツール酸塩は薬剤の100〜200 mgの割合で、総投与量が1 g以下になるまで投与されます。バルビツール酸塩の投与中、看護師は脈拍、血圧、呼吸の記録を保持します。 麻酔科医は、瞳孔の状態、眼球の動き、角膜反射の存在を監視して、麻酔のレベルを決定します。 バルビツール酸塩、特にチオペンタールナトリウムによる麻酔は、呼吸中枢の低下を特徴とするため、人工呼吸装置が必要です。 呼吸停止(無呼吸)が発生すると、呼吸装置マスクを使用して人工肺換気(ALV)が実行されます。 チオペンタールナトリウムの急速な投与は、血圧の低下と心臓の抑制につながる可能性があります。 この場合、薬の投与は中止されます。 手術では、バルビツレートによる単麻酔が、持続時間が 20 分を超えない短期間の手術に使用されます (例えば、膿瘍の切開、痰、脱臼の縮小、診断操作、および骨片の再配置)。 バルビツール酸の誘導体も導入麻酔に使用されます。 Viadryl (注射用プレディオン) は 15 mg/kg の用量で使用され、平均総用量は 1000 mg です。 Viadryl は、主に亜酸化窒素とともに少量で使用されます。 高用量では、この薬は血圧の低下を引き起こす可能性があります。 その使用の合併症は、静脈炎および血栓性静脈炎の発症です。 それらの発生を防ぐために、2,5%溶液の形で中心静脈にゆっくりと薬を投与することをお勧めします。 Viadrylは、導入型の麻酔として内視鏡検査に使用されます。 プロパニジド(エポントール、ソンブレビン)は、10%溶液5mlのアンプルで入手できます。 薬の投与量は7-10mg/ kgで、静脈内に素早く投与されます(全投与量は500秒で30mgです)。 すぐに眠りにつく-「針の先で」。 麻酔睡眠時間は5〜6分です。 目覚めは速く、穏やかです。 プロパニジドの使用は、意識を失った直後に起こる過呼吸を引き起こします。 無呼吸が時々発生することがあります。 この場合、換気は呼吸装置を使用して実行する必要があります。 マイナス面は、薬物投与を背景に低酸素症が形成される可能性です。 血圧と脈拍を制御する必要があります。 この薬は、小規模手術の外来手術における誘導麻酔に使用されます。 ヒドロキシ酪酸ナトリウムは非常にゆっくりと静脈内投与されます。 平均投与量は100-150mg/kgです。 この薬は表面麻酔を行うため、バルビツール酸塩(プロパニジド)などの他の麻薬と組み合わせて使用されることがよくあります。 誘導麻酔によく使用されます。 ケタミン(ケタラール)は、静脈内および筋肉内投与に使用できます。 薬の推定用量は2〜5 mg / kgです。 ケタミンは、単麻酔および導入麻酔に使用できます。 薬は表面的な睡眠を引き起こし、心血管系の活動を刺激します(血圧が上昇し、脈拍が速くなります)。 薬剤の導入は、高血圧患者には禁忌です。 低血圧患者のショックに広く使用されています。 ケタミンの副作用は、麻酔終了時および覚醒時の不快な幻覚である可能性があります。 4. 吸入麻酔 吸入麻酔は、容易に蒸発する(揮発性)液体 - エーテル、ハロタン、メトキシフルラン(ペントラン)、トリクロロエチレン、クロロホルム、またはガス状麻薬物質 - 亜酸化窒素、シクロプロパン - の助けを借りて行われます。 気管内麻酔法では、麻酔物質は麻酔器から気管に挿入されたチューブを通って体内に入ります。 この方法の利点は、気道の自由な開通性を提供し、首、顔、頭の手術に使用でき、嘔吐物、血液の誤嚥の可能性を排除するという事実にあります。 使用される薬物の量を減らします。 「デッド」スペースを減らすことでガス交換を改善します。 気管内麻酔は、主要な外科的介入に適応され、筋弛緩薬による多成分麻酔として使用されます(複合麻酔)。 少量のいくつかの薬の総使用はそれらのそれぞれの体への毒性効果を減らします。 現代の混合麻酔は、鎮痛、意識の遮断、リラクゼーションを提供するために使用されます。 鎮痛および意識のスイッチオフは、XNUMXつまたは複数の麻薬物質(吸入または非吸入)を使用して実行されます。 麻酔は、手術段階の最初のレベルで行われます。 筋弛緩、または弛緩は、筋弛緩薬の部分投与によって達成されます。 5. 麻酔の段階 麻酔にはXNUMXつの段階があります。 1.麻酔入門。 導入麻酔は、興奮の段階なしにかなり深い麻酔睡眠が発生する任意の麻薬物質を使用して実行できます。 ほとんどの場合、バルビツール酸塩、フェンタニルとソンブレビンの組み合わせ、ソンブレビンとの粉砕が使用されます。 チオペンタールナトリウムもよく使われます。 薬は1%溶液の形で使用され、400〜500mgの用量で静脈内投与されます。 誘導麻酔を背景に、筋弛緩薬を投与し、気管挿管を行います。 2. 麻酔の維持。 全身麻酔を維持するために、外科的外傷(ハロタン、シクロプロパン、酸素を含む亜酸化窒素)、および神経弛緩痛から体を保護できる麻薬を使用できます。 麻酔は手術段階の第 XNUMX 段階と第 XNUMX 段階で維持され、筋肉の緊張を取り除くために筋弛緩薬が投与されます。 したがって、現代の複合麻酔法の主な条件は、バッグや毛皮をリズミカルに圧迫するか、人工呼吸装置を使用して行われる機械的換気です。 最近、最も広まっている神経麻痺。 この方法では、酸素を含む亜酸化窒素、フェンタニル、ドロペリドール、筋弛緩薬が麻酔に使用されます。 静脈内導入麻酔。 麻酔は、酸素を含む亜酸化窒素を 2:1 の比率で吸入し、1 ~ 2 分ごとにフェンタニルとドロペリドール 15 ~ 20 ml を部分的に静脈内投与することによって維持されます。 心拍数の増加に伴い、フェンタニルが投与され、血圧が上昇します - ドロペリドール。 このタイプの麻酔は、患者にとってより安全です。 フェンタニルは鎮痛効果を高め、ドロペリドールは栄養反応を抑制します。 3.麻酔からの離脱。 手術が終了するまでに、麻酔科医は麻薬物質と筋弛緩薬の投与を徐々に停止します。 意識が患者に戻り、独立した呼吸と筋緊張が回復します。 自発呼吸の妥当性を評価するための基準は、ROの指標です2、RSO2、pH。 覚醒後、自発呼吸と骨格筋緊張の回復後、麻酔科医は患者を抜管し、回復室でさらに観察するために患者を搬送することができます。 6. 麻酔の実施を監視する方法 全身麻酔中、血行動態の主なパラメータは常に決定され、評価されます。 血圧、脈拍数を10〜15分ごとに測定します。 心臓血管系の病気を患っている人や胸部の手術では、心筋の機能を常に監視する必要があります。 脳波観察は、麻酔のレベルを決定するために使用することができます。 麻酔や手術中の肺の換気や代謝の変化を制御するには、酸塩基状態(RO)の研究を行う必要があります。2、RSO2、pH、BE)。 麻酔中、看護師は患者の麻酔チャートを維持します。これには、脈拍数、血圧、中心静脈圧、呼吸数、人工呼吸器のパラメーターなど、恒常性の主な指標が必ず記録されます。 このマップでは、麻酔と手術のすべての段階が固定されており、麻薬物質と筋弛緩薬の投与量が示されています。 輸血媒体を含む、麻酔中に使用されるすべての薬物が記録されます。 手術と薬の投与のすべての段階の時間が記録されます。 操作の最後に、使用されたすべての手段の総数が示され、麻酔カードにも反映されます。 麻酔および手術中のすべての合併症の記録が作成されます。 麻酔カードは病歴に埋め込まれます。 7. 麻酔の合併症 麻酔中の合併症は、不適切な麻酔技術または重要臓器への麻酔薬の影響により発生する可能性があります。 そのような合併症の XNUMX つに嘔吐があります。 麻酔の導入の開始時に、嘔吐は優性疾患の性質(幽門狭窄、腸閉塞)または嘔吐中枢に対する薬物の直接的な影響に関連している可能性があります。 嘔吐を背景に、誤嚥は危険です-胃内容物が気管と気管支に入る. 顕著な酸性反応を示し、声帯に落ちてから気管に浸透する胃内容物は、喉頭痙攣または気管支痙攣を引き起こし、その後の低酸素症を伴う呼吸不全を引き起こす可能性があります - これはいわゆるメンデルスゾーン症候群であり、チアノーゼ、気管支痙攣を伴います。頻脈。 危険なのは逆流 - 胃の内容物を気管や気管支に受動的に投げ込むことです。 これは通常、括約筋の弛緩と胃のオーバーフローを伴うマスクを使用した深い麻酔の背景に対して、または筋弛緩剤の導入後(挿管前)に発生します。 酸性の胃内容物の嘔吐または逆流中に肺に摂取すると、重度の肺炎を引き起こし、多くの場合致命的です。 嘔吐や逆流の出現を避けるために、麻酔の前にプローブで胃から内容物を取り除く必要があります。 腹膜炎と腸閉塞のある患者では、中程度のトレンデレンブルグ体位が必要ですが、プローブは麻酔全体を通して胃の中に残されます。 麻酔を開始する前に、Selick法を使用して、逆流を防ぐことができます。つまり、輪状軟骨を後方に押して、食道を圧迫します。 嘔吐が起こった場合は、綿棒と吸引で胃内容物を口腔から素早く取り除く必要があります。逆流の場合は、気管と気管支に挿入されたカテーテルを介して胃内容物を吸引して取り除きます。 嘔吐とそれに続く誤嚥は、麻酔中だけでなく、患者が目覚めたときにも発生する可能性があります。 このような場合の吸引を防ぐために、患者は水平またはトレンデレンブルグ体位を取り、頭を横に向ける必要があります。 患者を監視する必要があります。 気道の開通性が損なわれると、呼吸器系の合併症が発生する可能性があります。 これは、麻酔器の欠陥が原因である可能性があります。 麻酔を開始する前に、装置の機能、気密性、および呼吸ホースを通るガスの透過性を確認する必要があります。 気道閉塞は、深部麻酔中の舌の後退の結果として発生することがあります (麻酔の外科的段階のレベル III)。 麻酔中、固形異物(歯、プロテーゼ)が上気道に入る可能性があります。 これらの合併症を防ぐためには、深い麻酔を背景に下顎を前進させ、支える必要があります。 麻酔の前に、入れ歯を取り外し、患者の歯を検査する必要があります。 直接喉頭鏡検査による気管挿管の合併症は、次のように分類できます。 1) 喉頭鏡の刃による歯の損傷; 2)声帯の損傷; 3) 食道への気管内チューブの導入。 4) 右気管支への気管内チューブの導入。 5)気管からの気管内チューブの出口またはそれを曲げる。 記載されている合併症は、挿管技術の明確な知識と、気管の分岐部の上の気管内チューブの位置の制御 (肺の聴診を使用) によって防ぐことができます。 循環器系の合併症。 麻酔中および麻酔中の両方で、心臓の活動または血管運動中枢に対する麻薬物質の影響により、血圧が低下する可能性があります。 これは、麻薬物質(多くの場合、ハロタン)の過剰摂取で発生します。 低血圧は、麻薬物質の最適な投与量でBCCが低い患者に現れることがあります。 この合併症を防ぐために、麻酔前にBCCの赤字を埋める必要があり、手術中に失血を伴い、血液代替溶液と血液を輸血する必要があります。 心拍リズム障害 (心室頻拍、期外収縮、心室細動) は、さまざまな理由で発生する可能性があります。 1) 麻酔中の長時間の挿管または不十分な換気に起因する低酸素症および高炭酸ガス血症; 2)麻薬物質の過剰摂取-バルビツール酸塩、ハロタン; 3)カテコールアミンに対するハロタンの感受性を高めるハロタンのバックグラウンドに対するエピネフリンの使用。 心電図制御は、心臓のリズムを決定するために必要です。 治療は、合併症の原因に応じて行われ、低酸素症の解消、薬の投与量の減少、キニーネ薬の使用が含まれます。 心停止は、麻酔中の最も危険な合併症です。 その理由は、ほとんどの場合、患者の状態に対する誤った制御、麻酔技術の誤り、低酸素症、高炭酸ガス血症です。 治療は、即時の心肺蘇生からなる。 神経系からの合併症。 全身麻酔中、手術室での患者の体温調節と冷却の中心的なメカニズムに対する麻薬物質の影響の結果として、体温の適度な低下が許容されます。 麻酔後の低体温症の患者の体は、代謝の増加により体温を回復しようとします。 このような背景に対して、麻酔の終わりとその後に悪寒が現れ、これはハロセン麻酔の後に観察されます。 低体温症を防ぐには、手術室の温度(21〜22°C)を監視し、必要に応じて患者を覆い、輸液療法を行い、体温に温めた溶液を注ぎ、暖かく湿らせた麻薬を吸入する必要があります。 脳浮腫は、麻酔中の長期にわたる深い低酸素状態の結果です。 治療は直ちに行われるべきであり、脱水、過換気、脳の局所冷却の原則に従う必要があります。 末梢神経損傷。 この合併症は、麻酔後 90 日以上発生します。 ほとんどの場合、上肢と下肢の神経と腕神経叢が損傷しています。 これは、手術台での患者の位置が正しくない (腕を体から XNUMX° 以上外転させる、腕を頭の後ろに置く、腕を手術台の円弧に固定する、足を上に置く) ことの結果です。パディングなしのホルダー)。 テーブル上の患者の正しい位置は、神経幹の緊張を取り除きます。 治療は神経病理学者と理学療法士によって行われます。 講義番号13.局所麻酔 1. 表面麻酔 このタイプの麻酔は、麻酔物質を1つまたは別の器官、その表面と接触させることによって行われます。 この目的のために、コカインの3〜0,25%溶液、ジカインの2〜1%溶液、リドカインの2〜1%溶液、トリメカインの5〜0,5%溶液、およびピロメカイン溶液の2〜XNUMX%溶液。 ほとんどの局所麻酔薬は、不活性化されたナトリウム チャネルに結合し、膜脱分極中のナトリウム チャネルの活性化と細胞へのナトリウムの侵入を防ぎ、鎮痛効果を達成します。 表面麻酔の技術は単純で、潤滑、溶液の注入、または特別なスプレーガンを使用したスプレーで構成されています。 麻酔薬の作用の開始は pH に依存し、pH が低い場合は、pH が高い場合よりも効果が現れるまでに時間がかかります。 麻酔薬の作用の持続時間は、タンパク質への結合の程度によって異なります。 このタイプの麻酔は、診断操作および眼科、耳鼻咽喉科で使用されます。 2. 局所麻酔 局所麻酔には、神経叢、伝導、硬膜外、傍脊椎、およびその他の種類の麻酔が含まれます。 全身麻酔とは異なり、局所麻酔は、正常な生命機能を維持しながら、痛みの衝動を末梢で遮断するため、適切な外科的鎮痛を提供します。 局所麻酔は技術的に困難であり、神経叢または神経伝導体の解剖学的および地形学的位置に関する正確な知識、永続的な識別ポイント (骨突起、動脈、筋肉) の明確な方向付け、組織抵抗および患者の感覚を評価する能力が必要です。 痛みの感受性をオフにするには、トリメカイン (リドカイン) の 1% 溶液を導入するだけで十分であり、固有受容感覚をオフにして筋肉の弛緩を達成するには、より濃縮された局所麻酔薬溶液 (たとえば、トリメカイン 2-2,5% )。 感度の回復は逆の順序で行われます。つまり、最初に筋肉の緊張と固有受容感覚が現れ、次に痛みと温度の感覚が現れます。 局所麻酔薬の濃度と量が増えると、その毒性が高まることを考慮することが重要です。 最も広く使用されている溶液は、トリメカイン1〜2%、リドカイン1〜2%、ブピボカイン0,75〜0,5%です。 局所麻酔薬は、ミエリンを含まない細いミエリン繊維をより簡単かつ迅速にブロックします(すべての栄養素、および温度と痛みの刺激を行います)。 骨格筋、触覚受容器、固有受容器に向かう太いミエリン線維は、ランヴィエ絞輪の領域で局所麻酔の影響を受けるため、麻酔に対して非常に耐性があります。 麻酔薬の神経線維の脂質部分への拡散は急速ですが、神経の外側の濃度が神経自体の濃度よりも高くなるまでです。 この比率が変化した後、麻酔薬は神経から周囲の組織に反対方向に拡散します。 大量に投与された弱く濃縮された麻酔薬溶液は広く広がりますが、それらの拡散はごくわずかです。 少量で導入された濃縮溶液は、かなりの拡散度を持っています。 麻酔の効果は、経神経周囲に浸透し、適切な閾値ブロックを引き起こす麻酔薬の量に依存します。 投与される麻酔薬の濃度を1倍にすると、麻酔が3分の3延長され、9倍の量が導入されるとXNUMX〜XNUMX%しか延長されません。 局所麻酔薬はしばしばアナフィラキシー反応を引き起こします。 トリメカイン: 作用時間は 1 ~ 1,5 時間、最大単回投与量は 800 ~ 1000 mg リドカイン (キシカイン) は 1 ~ 2% 溶液で使用され、麻酔時間は最大 2,5 ~ 3 時間です。 ) 0,5-0,75 mg の最大単回用量で 150-170% 溶液で使用され、作用時間は 8-12 時間. 長時間作用型麻酔薬を使用する場合、リドカインを追加すると明らかに効果の発現が加速され、潜伏期。 局所麻酔を行うときは、一般的な規則を理解し、それに従う必要があります。 1)提案された麻酔の領域における神経叢および伝導体の解剖学的および地形学的特徴、ならびに麻酔を行う技術を明確に知っている; 2) 適切な局所麻酔薬を選択し、その濃度、総投与量、および神経叢または伝導体への送達方法を決定します。 3)患者の状態を評価し、アレルギーおよび薬物療法の背景を見つけます。 4)伝導および神経叢麻酔中の深い触覚および固有受容感覚の保存の可能性について患者に警告する。 5) 麻酔後の患者の血行動態と呼吸を常に監視する。 6) 麻酔の前または直後に、静脈穿刺を行い、起こりうる合併症を防ぐための措置を講じる。 7) 無菌および防腐措置に従って実施し、穿刺前に皮膚表面から化学的に活性な物質 (ヨウ素、クロルヘキシジンなど) を慎重に除去します。 8)局所麻酔薬を導入する前に、針が動脈血管に入るのを防ぐために吸引試験を実施することが不可欠です。 9) 局所麻酔中に患者が感じる感覚異常は、鎮痛を成功させるための前提条件であることを忘れないでください。 その不在は、失敗の可能性を示します。 10) 神経伝導体または神経叢の発見を容易にするために、針に負のインパルスを適用し、患者の体に固定されている電極の不関極に正のインパルス (陽極) を適用することにより、電気刺激を適用することをお勧めします。肌。 3. 頸神経叢 (ASP) の麻酔 片側または両側で行われるACSにより、銃創、怪我、腫瘍疾患の場合に、首、甲状腺、腕頭血管のすべての手術を行うことができます。 頸神経叢 (Plexus cervicalis) は、XNUMX つの上部頸神経 (C) の前枝から形成されます。1-から4)椎間孔からの出口で。 中斜角筋と肩甲骨を持ち上げる筋肉の前面にあり、頸椎の横突起の外側にあります。 頸神経叢の運動神経は首の筋肉を神経支配し、感覚神経は頭の後頭部の皮膚、首の前面と側面、耳介下領域をIおよびII肋骨のレベルまで神経支配します。耳介。 頸神経叢の最大の神経は横隔神経(p。prenicus)であり、Cから形成されます。3-から4 Cからの追加の分岐による頻度は低くなります5. ほとんどの感覚神経は、胸鎖乳突筋の後縁の下から中央に出て、首の表層、頭の後頭部の皮膚、および胸の上部で分岐します。 胸鎖乳突筋の中央の後縁に沿った頸神経叢の敏感な神経を麻酔する場合、首に多くの手術を行うことができますが、神経は筋肉に沿って吻合するため、麻酔は両側でなければならないことを覚えておく必要があります。首の正中線。 頸部の深層での大規模な手術(ストラム切除、頸部腫瘍の除去、喉頭切除、頸動脈内膜切除など)の場合、前方アプローチで頸神経叢を麻酔する必要があります。 側方アクセスでは、重篤な合併症(硬膜下腔への麻酔薬の導入)のリスクがあるため、使用されません。 前方アプローチでASSを実行するには、患者が首の下に小さなロールを付けて仰向けになる必要があります。 頭は平らに横たわり、回転せずに正中線にまっすぐにするか、穿刺と反対の方向にわずかに回転させる必要があります。 体に沿って手、麻酔科医は穿刺の頭に立っています。 ランドマーク: 胸鎖乳突筋、舌骨、内頸動脈、下顎角。 麻酔法 胸鎖乳突筋の前方、下顎角の 2 cm 下で、内頸動脈の拍動を測定します。 舌骨の水平枝は、椎骨Cの横突起のレベルに対応します3. 針の注射点は、舌骨の水平枝の続きである線と、胸鎖乳突筋の前縁との交点にあります。 この交点で、無菌条件下で「レモンの皮」が形成され、注射針が外側から内側、前から後ろに向けられ、胸鎖乳突筋の内側と内頸動脈の後ろに進みます。動脈 (胸鎖乳突筋と触知可能な内頸動脈の間のギャップ) 患者が感覚異常を発症するか、針が椎骨 C の横突起に当たるまで3。 注射の深さは2〜5cmを超えません。針はこの位置にしっかりと固定され、吸引テストが実行され、針の端が血管の内腔にあるかどうかが判断されます。 麻酔のために、トリメカインの10%溶液12〜2mlを両側から注射します。 頸神経叢の麻酔を強化するために、首の前面に向かう表在枝をさらにブロックすることができます。 それらの出口の場所は、胸鎖乳突筋の後縁の中央です。 針は、首の表在筋膜の下の出口点に注射されます。 2% トリメカイン溶液を 3 ~ 5 ml の量で頭側および尾側 (扇形) に投与します。 十分な麻酔は 8 ~ 12 分後に発生し、ほとんどの患者で 1,5 ~ 2 時間以内に効果的な鎮痛が得られます。 合併症 ホルネル症候群、横隔神経ブロック、反回神経麻痺、麻酔薬の血管内注射による低血圧。 嗄声は頸神経叢ブロックの主な症状です。 側方アクセスの最も危険な合併症は、高度な脊椎麻酔の発生と、IV 心室の空洞への麻酔薬の侵入です。その症状は、眼球中枢の麻痺、瞳孔拡張、血圧の低下、呼吸不全、筋弛緩です。 . 頸神経叢の麻酔の絶対禁忌は、反対側の横隔神経の麻痺、頸神経叢の神経の損傷です。 4. 腕神経叢 (APS) の麻酔 APSを使用すると、上肢、肩関節、肩、前腕、手のすべての手術を行うことができます:切断、骨片の再配置と固定による創傷の外科的治療、血管と神経の手術、肩の脱臼の縮小など. 特に戦時中の上肢への外科的介入の頻度が高いため、これらの手術中の合理的な麻酔方法の問題が生じます。 地形的には、腕神経叢には鎖骨上動脈と鎖骨下動脈の2つの部分があります。 枝は鎖骨上部分から首の深い筋肉と肩甲帯の筋肉まで伸びています。 上腕神経叢の鎖骨下部分は、腋窩動脈を内側、背面、外側から覆うXNUMX本の幹で構成されています。 長い神経は体幹から始まり、上肢の自由な部分に行き、XNUMXつの短い神経は肩甲帯に行きます。 内幹から尺骨神経と下根を正中神経に向けて出発します。 橈骨神経と腋窩神経は後部幹から離れ、筋皮神経と正中神経の上根は外幹から離れます。 したがって、腕神経叢の麻酔は、鎖骨上、腋窩、鎖骨下のアプローチを使用してさまざまな方法で可能です。 鎖骨上アプローチの中で、間質腔での麻酔法は、最も単純で信頼性が高く、合併症が少ないものとして最も広く使用されています。 ウィニーによる腕神経叢麻酔 患者は仰向けになり、頭を穿刺部位とは反対の方向に向け、あごを反対側の肩帯に持ってきます。 穿刺の側面からの手は体に沿ってあり、わずかに引き下げられています。 ランドマーク: 胸鎖乳突筋、前斜角筋、間質腔、外頸静脈、鎖骨、輪状軟骨。 麻酔技術。 皮膚は消毒液で処理されます。 頭のわずかな隆起ではっきりと輪郭を描く胸鎖乳突筋の後ろで、輪状軟骨のレベルで、左手の指先が前斜角筋に置かれます。 前斜角筋と中斜角筋の間で指を横方向にさらに0,5〜1,5 cm変位させて、斜角筋間のギャップを調べます。 これは斜角筋を緊張させるので、深呼吸でよりはっきりします。 間質腔の深さでは、頸椎の横突起が触診され(強い抵抗感)、指先での圧力が高まると、肩や肩甲帯の知覚異常が引き起こされることがよくあります。 より尾側では、間質腔では、鎖骨下動脈を触診することができます。 上部の間質腔は外頸静脈と交差しています。 針注射点は、輪状軟骨の高さで間質腔の上部にあります。 この時点で、「レモンクラスト」が形成され、それを通して針が内側にいくらか下向きに、前から後ろに(背側方向に)横方向のプロセスCに向けられます。6 矢状面に対して 30° の角度で。 針が1,5〜4 cmの距離で内側に進むと、感覚異常が発生し、針の先端が第6頸椎の横突起にかかります。 この位置で、針を固定または 1 ~ 2 mm 引き上げ、吸引テストの後、トリメカイン (リドカイン) の 30% 溶液またはブピボカイン (マルカイン) の 40 ~ 2% 溶液を 0,5 ~ 0,75 ml 採取します。注射した。 局所麻酔液の最初のミリリットルの導入中に、患者は針先の正しい位置を示す短期間の痛み (「電気ショック」) を経験します。 感覚異常がない場合、針先の位置は、冷蔵庫から取り出した 0,5% 塩化ナトリウム溶液 0,9 ml を導入することによって確認できます。 上肢の痛みの出現は、冷たい溶液が神経と接触していることを示しています。 禁忌:反対側の反回神経または横隔神経の麻痺、腕神経叢の神経の損傷。 合併症の可能性:特に椎骨動脈への局所麻酔液の血管内注射、その急速な拡散がCNS中毒につながります。 麻酔液のくも膜下投与は完全な脊椎ブロックを引き起こします。 硬膜外投与は、高度の硬膜外麻酔をもたらします。 S. V. Gavrilin および L. G. Tikhonov の方法による間質腔内の腕神経叢の麻酔 この方法と他の方法の主な違いは、穿刺部位に胸膜のドームと大きな血管がないことです。 患者は仰向けになり、頭を穿刺部位とは反対の方向に向け、あごを反対側の肩帯に持ってきます。 小さなローラーが肩の下に置かれ、穿刺の側面からの腕が体に沿って横たわっています。 ランドマーク: 鎖骨、胸鎖乳突筋。 麻酔技術。 針の注射点は、鎖骨の中央の上端から復元された垂線の上部にあり、その長さは胸鎖乳突筋の長さの60/6です。 この時点で、「レモンの皮」が形成され、筋肉内注射針が皮膚表面に対して6°の角度で挿入されますが、針と仮想または垂直に描かれたものは同じ平面にある必要があります。 上肢に知覚異常が現れるまで、第1頸椎の横突起の方向に針を挿入します。 知覚異常がない場合、針は第2頸椎の横突起まで完全に進められ、30〜40 mm引き寄せられた後、トリメカインまたはリドカインの2%溶液2〜5mlが注入されます。 。 針の挿入深さはXNUMX-XNUMXcmです。 V. S. Sokolovskyの修正における腕神経叢の麻酔 患者は仰向けになり、頭は正中線にあり、腕は体に沿って横になります。 ランドマーク: 胸鎖乳突筋と鎖骨。 麻酔技術。 首の皮膚上の点を見つけやすくするために、麻酔側の胸鎖関節の領域に頂点を持つ三角形が作成されます。 三角形の光線は鎖骨の軸であり、乳様突起と胸鎖関節を結ぶ直線です。 鎖骨の中央から角度ABCの二等分線に垂線が復元されます。 交点は、手術台の水平面に対して45°の角度で、頸椎の軸に垂直に進む針の注射点です。 深さ2〜3cmで、知覚異常を受けて吸引試験を行った後、トリメカイン(リドカイン)の30%溶液40〜2mlを注射します。 麻酔は10〜12分で行われます。 決定的な知覚異常が得られた場合、電気刺激を使用して頸神経叢の神経幹を特定することが望ましい。 5.手首領域の末梢神経の麻酔 手の手術では、尺骨神経、正中神経、橈骨神経を麻酔する必要があります。 いずれの場合も、針は手首の近位襞のレベルで注入されます。 麻酔中、患者は仰向けになり、手首の領域で、腕は回外し、わずかに曲がります。 ランドマーク: 尺骨茎状突起、豆状突起、尺側手根屈筋腱、および長手根屈筋腱。 尺骨神経の麻酔 尺骨神経のトポグラフィー。 前腕の下3分の5では、尺骨神経は尺側手根屈筋の外側と尺骨動脈の内側を走っています。 手首の高さまたは前腕の屈筋表面で、手首の2〜5 cm近位で、尺骨神経は背側と掌側のXNUMXつの枝に分かれます。 背側枝は敏感で、手の尺骨屈筋の腱の下に入り、ほぼ手首の関節の高さで手の甲の皮下組織に出ます。 橈骨神経の枝と吻合し、XNUMX½本の指を神経支配します。 尺骨神経の掌側枝は混合されており、豆状骨のレベルで、深部と表面のXNUMXつの枝に分かれています。 後者は敏感であり、XNUMX番目の指の小指球領域と薬指の尺骨側を神経支配します。 尺骨神経の手掌枝の麻酔のための技術。 針の注射点は、手の尺骨屈筋の腱の内側にある手首の近位襞のレベルです。 1-2 cm の深さの針は、豆状骨に向かって皮下組織を通過します。 感覚異常の出現後、吸引試験が陰性の場合、針を固定し、3%トリメカイン溶液5〜2mlを注射します。 知覚異常がない場合、針が骨に接触するまで針を進め、針を抜くと、組織に 2% トリメカイア溶液を浸透させます。 尺骨神経の背側枝の麻酔のための技術。 針の注射点は、手首の近位襞と尺骨屈筋の腱の内側縁との交点のレベルにあります。 針は尺骨の茎状突起に向けられます。 感覚異常を得るために、トリメカインの3%溶液5〜2mlを注射します。 感覚異常がない場合、針を抜き取り、5% トリメカイン溶液 10 ~ 2 ml を組織に浸透させます。 合併症はありません。 正中神経麻酔 患者は仰向けになり、腕を回外してまっすぐにします。 ランドマーク: 長掌筋の腱、手の橈骨屈筋の腱、および手首の近位皮膚襞。 地形。 前腕の下 4 分の 5 では、正中神経が皮膚の表面に非常に近く、筋膜の下、遠位皮膚襞の約 1 ~ 2 cm 上にある内側溝を通過します。 内側の溝は、尺骨側の手の橈骨屈筋の腱によって外側から形成されます - 手の長い屈筋の腱によって。 正中神経の枝は、第 3、第 4、第 XNUMX 指、および第 XNUMX 指の外側表面、ならびに母指球の筋肉を支配します。 麻酔技術。 針の注射点は、長掌筋の腱と手の橈骨屈筋の間の手首の近位皮膚襞の線上にあります。 針を皮下組織を通して0.5~1cmの深さまで垂直に前進させ、知覚異常を得た後、針を固定し、3~5mlの2%リドカイン溶液を注射する。 深さ 0,5 cm の感覚異常を達成できない場合は、ゆっくりと針を抜きながら、組織に 1% トリメカイン溶液 3 ~ 5 ml を扇形に浸潤させます。 橈骨神経の麻酔 ランドマーク: 橈骨の茎状突起、橈骨動脈、「解剖学的嗅ぎタバコ入れ」。 地形。 橈骨神経の表在枝は、まず橈骨動脈とともに前腕に至り、手首関節から約8cmの距離にある前腕の下1分の2で、神経は腕橈骨筋の腱と交差し、前腕の後面に到達し、そこで遠位および後方に進み、大指の長い外転筋と短い伸筋を横切ります。 「解剖学的嗅ぎタバコ入れ」の上部にある手首の高さで、指 3、XNUMX と指 XNUMX の外面を刺激する末端枝に分かれます。 XNUMX つの神経すべての枝は、しばしば前腕、手首、および手で互いに吻合します。 麻酔技術。 注射点は、「解剖学的な嗅ぎタバコ入れ」の上部の投影で橈骨動脈の外側の手首の近位皮膚襞のレベルにあり、注射され、針は「嗅ぎタバコ入れ」に向けられます。 感覚異常が現れたら、針を固定し、負の吸引試験で、3〜5mlの2%トリメカイン溶液を注射します。 感覚異常がない場合、トリメカインの 5% 溶液 10 ~ 2 ml を下層組織に扇形に注入し、短伸筋および長外転筋の腱から長さ 3 ~ 3,5 cm の浸潤「ブレスレット」を作成します。片側の親指、親指の長い伸筋 - もう一方の側。 6.下肢の麻酔 下肢に外科的介入を行うには、XNUMX つの主要な神経すべてに麻酔をかける必要があります。 それらのうちのXNUMXつ - 大腿部、閉鎖神経、および大腿部の外皮神経 - は腰神経叢に由来し、坐骨神経は部分的に腰椎および仙骨神経叢のXNUMXつの枝から形成されます。 各神経は、下肢の特定の領域を神経支配します。大腿神経 - 大腿部の前面、下肢の前面内面、および足の後部。 坐骨 - 下肢の後面および側面、足の底表面およびその外縁、閉塞具 - 大腿の内面; 大腿部の外皮神経 - 大腿部の側面。 深い感受性のゾーンは、皮膚ゾーンの神経支配と一致します。 下肢のすべての筋肉は、閉鎖神経によって神経支配される外転筋群を除いて、大腿神経および坐骨神経から運動線維を受け取ります。 膝関節とその前面は大腿神経、内面は閉鎖孔、外側は外皮神経と坐骨神経、後面は後皮神経、大腿神経と坐骨神経によって支配されています。 前方(鼠径)アクセスによる腰神経叢の麻酔 患者は仰向けになります。 ランドマーク:鼠径靭帯と大腿動脈。 地形。 腰神経叢は、L根の前枝を吻合することによって形成されます。1-L2-L3 部分的に Th の前枝によって12 とL4 神経。 神経叢は腰椎の横突起の前に位置し、腰の四角筋 - 背側、大腰筋 - 腹側、椎体 - 内側、筋肉の枝を放ち、筋膜に下降しますベッド。 腰椎神経は、交感神経幹の腰椎節と枝を接続しており、運動神経線維、感覚神経線維、および交感神経線維を含んでいます。 腰神経叢の最大の神経は、外大腿皮神経 (L2-L3)、栓子 (L2-L4) および大腿骨 (L2-L4)神経。 後者は腰神経叢の続きであり、腸骨靱帯によって内側に位置する大腿動脈から分離され、筋肉のラクナを通って腓腹靱帯の下の大腿部まで伸びます。 この場所の大腿神経の幅は約 0,7 ~ 0,8 cm、大腿神経の深さは平均 1,8 ~ 3 cm、-0,5 cm で、鼠径靭帯の下で神経は 1 つの束を形成します。 前脚の枝は、大腿四頭筋、膝関節の中央および内側を神経支配し、伏在神経に入り、下肢の内側表面および足首の内側を神経支配します。 坐骨神経の麻酔により、膝関節の下の任意の領域で手術が可能になり、大腿骨頸部の骨折を除く下肢の骨のすべての骨折を軽減します。 麻酔技術。 皮膚は消毒液で処理されます。 「レモンの皮」を麻酔液で形成し、その後、針を鼠径靭帯の下 1 ~ 1,5 cm、触診した大腿動脈の外側 0,5 ~ 1 cm に注射します。 針は、皮下組織を通して鼠径靭帯の下でやや近位方向に向けられます。筋膜の穿刺後3〜4 cmの深さで、針は抵抗の喪失で失敗し、感覚異常が発生し、前面に伸びます太ももの。 この位置で、左手の親指と人差し指で針を固定し、左手の手のひらの端を、針の遠位側の大腿部の軟部組織に力を加えて押し、35 ~ 40 ml の液体を注入します。 1,5% トリメカイン溶液を注射します。 軟部組織への圧力は 1,5 ~ 2 分続きます。 したがって、クランプによる大腿神経の麻酔は、前方アプローチから実行される腰神経叢の麻酔に変わります。 麻酔の作用は2〜2,5時間続きます。 合併症:腰神経叢の麻酔が坐骨神経の麻酔と組み合わされた場合、1回の総投与量がXNUMXgを超えると、麻酔薬のかなり急速な吸収が可能です。 腰神経叢の麻酔は、大腿骨 (L2-L4) と閉鎖神経 (L2-L3)、生殖大腿神経(L1-L2) と外側大腿皮神経 (L2-L3)。 麻酔中の患者の体位は、脚を曲げた健康側です。 ランドマーク: 第 4 腰椎の棘突起 (背後の腸骨稜を結ぶ線)。 第 3 腰椎の棘突起から棘突起の頂上に沿って尾側に 4 cm、最後の点から外側に 5 cm。 麻酔技術。 尾側方向の第 4 腰椎の棘突起から、長さ 3 cm の線が引かれ、その端から長さ 5 cm の垂線が横方向に上向きに復元されます。注射針のポイントです。 「レモンの皮」を作成した後、長さ 12 ~ 15 cm の針を、第 5 腰椎の横突起に接触するまで皮膚に垂直に挿入します。 頭側では、第5腰椎の横突起から滑り落ち、針が四角腰筋の厚さに入ります。 同時に、注射器で溶液を注入するのに抵抗が感じられます(または、注射器内の気泡の変形に伴って弾力的な抵抗が発生します)。 「抵抗がなくなった」(気泡が変形しない)感覚のある深さまで針を通す。 このテストは、針が方形腰筋と大腰筋の間の筋膜にあることを示します。 針はこの深さに固定され、麻酔を達成するために 35 ~ 40% トリメカイン (リドカイン) 溶液 1,5 ~ 2 ml が注入されます。 可能性のある合併症:針の間違った位置での局所麻酔薬の筋肉内注射、および濃縮液が注射されたときの血液への麻酔薬の急速な再吸収。 前方アプローチからの坐骨神経の麻酔 地形。 坐骨神経は仙骨神経叢(L4-S3)。 それは小さな骨盤で形成され、動脈とともに梨状開口部を通って骨盤腔を出ます。 その内側には、内陰部動脈、静脈、および陰部神経からなる神経血管束と同様に、後皮神経が通過します。 臀部では、坐骨神経は大殿筋の下、ジェメリス、内閉鎖筋、および大腿四頭筋の後ろにあります。 後者では、それは坐骨結節と大腿骨の大転子からほぼ等しい距離にあります。 原則として、膝窩の上部で、神経は末端の枝、つまり脛骨神経と総腓骨神経に分かれます。 脛骨神経は、膝窩静脈および動脈の外側および表面に位置する膝窩窩の中央を通過し、血管とともに足首膝窩管に入ります。 脛骨神経は、下腿の後面の筋肉群、足の裏のすべての筋肉、下腿の後面の皮膚、かかと、および足の外側縁を神経支配します。 坐骨神経から股関節に枝分かれします。 臀部のひだの領域では、大腿二頭筋の長頭から外側の太ももの広い筋膜の下に表面的に位置しています。 総腓骨神経は、腓骨頭の周囲の膝窩の外側に沿って走っています。 それから、膝関節と下腿の側面の皮膚への枝があり、下腿の筋肉、足の裏の筋肉、つま先の後ろの皮膚も神経支配します。 坐骨神経の麻酔は前方から行います。 ランドマーク: 上前腸骨軸と大腿骨大転子の最も突出した部分。 麻酔技術。 患者を仰向けに寝かせ、上前腸骨棘と大腿骨大転子の最突出点を直線で結び、最後の点から大腿前面に垂線を戻す。 垂線の長さは、上前腸骨棘と大腿骨大転子との間の距離に等しく、この垂線の終点が投影点です。 下肢の生理的位置で、皮膚を消毒液で処理し、「レモンの皮」を作成した後、長さ 12 ~ 15 cm の針を、大腿骨の小転子に当たるまで垂直に下に向けます。 針が小転子から滑り落ちた後、主な方向を変えずに、針はさらに深く運ばれます-感覚異常が発生するまで4〜5 cm。 感覚異常を達成できない場合は、針を骨に戻し、手足を7〜10°内側に回して、患者に感覚異常が現れるまで針を再び進めます。 後方アプローチからの坐骨神経の麻酔 麻酔技術。 患者は健康な側に横たわり、麻酔をかけた手足を股関節と膝関節で 45 ~ 60° の角度で曲げます。 大腿骨大転子の最も突出した部分から、上後腸骨棘まで直線が引かれ、その中央から、長さ4〜5 cmの垂線が尾側方向に下げられます。坐骨神経の投影点として。 針は、患者の体の前頭面に対して 90° の角度で注入され、知覚異常または骨との接触が得られるまで進められます。 必要に応じて、針を引き上げて、元の注射の外側または内側に約 0,5 cm 挿入します。 感覚異常を取得する必要があります。 リドカイン (トリメカイン) の 20% 溶液を 25 ~ 2 ml 入れます。 患者がうつ伏せになっても、麻酔の技術は変わりません。 膝窩の麻酔 下肢と足の外科的介入では、膝窩の脛骨神経と腓骨神経を麻酔するだけで十分です。 患者の位置 - 健康側または胃の上。 ランドマーク: 上腕二頭筋の腱、太ももの半膜様筋および半腱様筋、膝蓋骨、ふくらはぎの筋肉。 地形。 膝窩には繊維、血管、神経、リンパ節が含まれています。 上部外側境界は大腿二頭筋の腱によって形成され、上部内側境界は半膜様筋と半腱様筋の腱によって形成され、腓腹筋の外側頭は下と外側にあり、下部内部は内側です腓腹筋の頭。 膝窩の上角の投射は、坐骨神経の菱形窩の上隅にある膝蓋骨の上端にほぼ対応し、脛骨神経と総腓骨神経に分けられます。 後者は上端から腓腹筋の外側端に行き、腓骨頭の首を半らせん状に包み込みます。 膝窩では、脛骨神経が正中線に沿って最も表面的に通過し、静脈がそこからより深く内側にあり、さらに深く内側の骨に近いところに膝窩動脈があります。 麻酔技術。 菱形窩の上隅は、膝蓋骨の上端のレベルにあります。 注射点は、大腿二頭筋の腱によって外側から形成され、大腿の半膜様筋および半腱様筋の腱によって内側から形成された、この角度から下げられた二等分線の上部角度の1〜1,5 cm下にあります。 針の動きの方向は、脛骨神経の感覚異常が得られるまで、腹臥位の患者に対して厳密に垂直です。 知覚異常がない場合、針は扇形に向けられ、毎回皮下組織のレベルまで引き上げられます。 吸引試験の後、トリメカインの5%溶液10〜2mlを注射します。 同じ点から総腓骨神経を遮断するために、針は前頭面に対して 30 ~ 45° の角度で横方向に向けられます。 感覚異常を受けた後、トリメカインの5%溶液10〜2mlを注射します。 合併症や禁忌はありません。 局所麻酔の合併症 RAの間、合併症はめったに発生せず、XNUMXつのグループに分けることができます。 1.具体的で、方法論の技術的なエラーに関連しています。 1) 脊柱管または硬膜外腔への局所麻酔薬の静脈内または動脈内への誤った注入 (頸神経叢の麻酔、鼠径アクセスによる腰神経叢の麻酔を伴う); 2)空洞および臓器(胸膜腔、肺)の穿刺。 3)穿刺を怠り、大きな血管に損傷を与える血腫の形成。 血腫は周囲の組織または神経血管束を圧迫します。 4) 局所麻酔薬の急速な再吸収に伴って起こる長期にわたる重度の低血圧; 5)乱暴な操作中に注射針の端で神経叢または伝導体に外傷を負った。 6)神経叢または伝導麻酔後の鎮痛効果の欠如。 2.非特異的で、主に局所麻酔薬の作用に対する身体の一般的および局所的反応によって、毒性およびアレルギー反応の形で現れます。 麻酔薬の投与時間、投与量、部位によっては、非特異的な合併症が発生することがあります。 この場合、中枢神経系または心血管系の病変が優勢です。 中枢神経系の側からの合併症は、軽度(中枢神経興奮のみに限られる)または重度であり、中枢神経系の抑制によって完全な麻痺の可能性が示されます。 非特異的合併症の性質: 1) トリメカインまたはリドカインの動脈内または静脈内への大量 (1 g 以上) の同時投与を伴う麻酔薬の過剰摂取。 局所麻酔薬の血管内注射では、毒性反応がすぐに現れ、薬物の過剰摂取では10〜15分後に現れます。 局所麻酔薬の過剰投与による重度の中毒反応は非常にまれです。 はるかに頻繁に(死ぬまで)、局所麻酔薬の高濃度溶液の血管内投与で観察されます。 2) 中枢神経系および心血管系の障害の複合症状を特徴とする局所麻酔薬の導入に対するアレルギー反応: 不安、意識障害、言語障害、筋肉のけいれん、痙攣、深呼吸、心臓リズム障害、QR 拡張、血圧を下げる、頻脈、無呼吸、心静止; 3)麻酔部位での手術野の質の悪い処理、注射器、針および溶液の不十分な滅菌、ならびに局所皮膚感染症(膿皮症)の存在による感染性合併症意図的な操作; 4)神経叢および伝導麻酔による低血圧の発症は、硬膜外麻酔および脊椎麻酔よりもはるかに一般的ではありませんが、これは循環血液量減少を修正する重要性を低下させません。 5) 少数の症例で局所麻酔薬の濃縮溶液を導入すると、徐脈の発症が認められますが、これは硫酸アトロピンによって十分に阻止されます。 心室細動や心停止の症例は非常にまれです。 実施の禁忌 禁忌は次のとおりです。 1.ヒステリー。 2.悪化する傾向。 3.神経学的合併症:麻酔の提案された領域の片麻痺および片麻痺、脊髄の疾患、多発性硬化症、末梢神経の疾患。 4.針注射点の領域の皮膚の感染症。 5. 敗血症。 6.大量の失血後の出血および重度の循環血液量減少の傾向。 7.悪性貧血(相対的禁忌)。 7. 硬膜外麻酔 その本質は、硬膜外腔に麻酔薬を導入して脊髄神経とその根を遮断することにあります。 実施技術と麻酔ゾーンは講義2に示されています。 鎮痛の用量と期間 1.リドカインは4ml(2%)の量で注射され、麻酔の持続時間は4時間です。 2. マルケインは 6 ~ 10 ml (0,5%) の用量で投与され、麻酔時間は 6 ~ 8 時間です。 3.ナロピンは4〜6ml(1%)の用量で投与され、麻酔の持続時間は4〜6時間です。 このタイプの麻酔では、血行動態が損なわれ、血圧が急激に低下します。 したがって、このタイプの麻酔を使用する場合は、患者の圧力を常に監視し、必要に応じてその補正が必要です。 8.腰椎麻酔 このタイプの麻酔は、脊柱管に麻酔薬を注入することによって達成されます。 腰椎穿刺の手技は講義No.2で説明します。特徴は、穿刺のレベルが高いことです(T12-L1、L1-L2)そして針からマンドリンを取り除いた後、すぐに麻酔薬が注入されます。 麻酔薬の量は3〜5mlです。 ナロピンは0,5%の濃度で、リドカインは2%、マルカインは0,5%で投与されます。 麻酔の持続時間は 4 ~ 6 時間で、このタイプの麻酔も重度の低血圧を引き起こします。 高レベルの麻酔 (T12-L1) 呼吸器系の問題を引き起こす可能性があります。 最も一般的な合併症は頭痛です。 9. A. V. ヴィシネフスキーによる頸部迷走交感神経遮断 患者は、提案された封鎖の側の手がテーブルの端にぶら下がるように、仰向けにテーブルに置かれます。 胸鎖乳突筋を弛緩させる必要があります。 肩帯の下にローラーを置き、頭を反対方向に引っ込めます。 この位置では、首の解剖学的輪郭がはっきりと描かれています。 フィールドは、アルコールとヨウ素による潤滑で処理されます。 医者は同じ名前の封鎖の側に立っています。 注射部位は、胸鎖乳突筋の後縁と静脈との交点によって形成される角度です。 左手の人差し指は、胸鎖乳突筋の後縁、外頸静脈と交差する場所の上に置かれます。 この場所を指で強く押して、神経血管束を正中線に動かそうとします。 この場合、指は頸椎の前面を容易に感じます。 針の注入とその前進は、脊椎の前面に焦点を合わせながら、ゆっくりと上向きと内側に行う必要があります。 針は、注射の安全性を確保するために、少量 (2 ~ 3 cm) で送信される 0,25% ノボカイン溶液に沿って移動します。 注入中の注射器は、コントロール(血液)の目的で繰り返し針から抜かれます。 針を椎骨に持ってきて、針がどのように支えられているかを感じます。 次に、針への圧力が弱まり、それにより針が1〜2 mm離れます。その後、40〜60 mlの溶液が注入され、椎骨前腱膜に沿って忍び寄る浸潤に広がり、交感神経の迷走神経を覆います、そしてしばしば横隔神経、胸膜肺領域からの刺激の伝達を遮断(ブロック)します。 迷走交感神経遮断の有効性は、ホルネル症状 (瞳孔の狭小化、眼瞼裂の狭小化、および眼球の退縮) の出現によって証明されます。 呼吸リズムと脈拍が少なくなり、息切れとチアノーゼが減少し、全身状態が改善します。 針が首の血管に入らないようにするには、下にある神経血管束のある胸鎖乳突筋を人差し指で正中線まで十分に強く動かす必要があります。 針を水平方向に動かすと、脊椎前腱膜の下に解決策が導入され、その後、日中止まらない痛み症候群の形で合併症が発生する恐れがあるため、針を上向きおよび内向きにすることが重要です。 講義番号14.患者の重症度の評価とモニタリング 患者の身体状態の評価。 1ポイント - 病気が限局性であり、原則として全身性障害を引き起こさない患者、つまり 実質的に健康な人。 2ポイント-これには、恒常性の顕著な変化なしに体の生命活動を中程度に混乱させる発現されていない障害のある患者が含まれます。 3つのポイント-身体の機能を著しく破壊するが、障害を引き起こさない重要な全身性障害のある患者。 4点 - 人命に大きな危険をもたらし、障害につながる重度の全身性障害の患者。 5ポイント-状態が重大であると考えられる患者、24時間以内に死亡するリスクが高い。 外科的介入の量と性質: 1ポイント - 小規模な手術:表面に位置する腫瘍と局所的な腫瘍の除去、小さな膿瘍の開放、指とつま先の切断、痔核の結紮と除去、合併症のない虫垂切除術とヘルニア切開術。 2点-中等度の重症度の手術:長期の介入を必要とする表面に位置する悪性腫瘍の除去。 空洞に限局した膿瘍の開口部; 上肢および下肢の切断および関節離断; 周辺船の操作; 広範囲の介入を必要とする複雑な虫垂切除術およびヘルニオトミー; 試験開胸術および開腹術; 複雑さと介入の範囲が類似しているものもあります。 3 ポイント - 広範な外科的介入: 腹部臓器に対する根治的手術 (上記のものを除く)。 胸腔の臓器に対する根本的な手術; 経腸仙骨切断などの拡張四肢切断; 脳外科手術。 4つのポイント-心臓、大血管、および特別な条件下で実行されるその他の複雑な介入(人工循環、低体温など)の操作。 緊急の外科的介入は、計画されたものと同様に、身体の状態と手術の量に応じて評価されますが、別のグループに含まれるか、インデックス「C」によって図に加えて示されます。 注意 手術および麻酔のリスクは次のように指定されます。分子は初期状態の重症度をポイントで示し、分母は手術の量をポイントで示します。 米国麻酔科学会 (ASA) によって開発された、患者の客観的な状態の分類。 1.全身性疾患はありません。 2. 機能障害のない軽度の全身性障害。 3.機能障害を伴う中等度および重度の全身性疾患。 4. 常に生命を脅かし、機能不全に至る重度の全身性疾患。 5.終末期、手術に関係なく日中の死亡リスクが高い。 6. 脳死、移植のための臓器提供。 介入が緊急に行われる場合、状態の評価は文字「E」で補足されます。 患者の状態の評価と各症例の致死率を表 7 に示します。 表7 患者の状態と周術期死亡率の評価
モニタリング (表 7) は、機能とプロセスの制御、特に麻酔や集中治療中の合併症を防ぐための危険な逸脱の特定です。 監視は、以下を制御するために実行されます。 1)患者の機能(心電図検査、パルスオキシメトリ、カプノグラフィなど)。 2) 治療作用 (神経筋ブロックの制御); 3) 環境 (吸入混合物のガス組成); 4)技術的手段(人工呼吸器など)の操作。 複雑度による機能の監視は、次の方法で実行できます。 1)パラメータの継続的な監視。 2)パラメータが確立された制限を超えて失敗した場合のシグナリングによる制御。 3) パラメーターが設定された制限を超えた場合の通知による継続的な監視と、さらに解決策のヒント。 4) 機能正常化対策の実施についても同様。 監視の妥当性は、次の理由によるものです。 1)外科的介入の複雑さと期間がますます増大している。 2)患者の機能障害の重症度の増加; 3)重要な医療で使用される技術的手段の複雑さ。 モニタリングの意義: 1) 障害のタイムリーな診断と、心停止や呼吸停止を含む重篤な合併症の予防; 2)集中治療と高効率の治療のより適切な戦術。 モニタリングの徴候: 1) 最小限のモニタリング - 麻酔中および集中治療中は常に必須です。 2)身体機能の重大な違反の場合、特に患者が多臓器不全を発症した場合の詳細なモニタリング(非侵襲的および侵襲的方法)。 3) 予防的モニタリング - 重大な状態を発症するリスクがあります。 監視基準。 1978年、オランダ安全委員会は、監視に必要な機器をリストした最初の手術室監視基準を導入しました。 1985年、保険会社の提案により、ハーバード大学の麻酔科モニタリング基準が提案されました。これは、手術中の麻酔中の患者をモニタリングするためのパラメータと、そのようなモニタリングのモードを提供します。 実践への導入により、麻酔合併症のリスクが軽減され、患者にとってより安全になりました。 1997 年にロシアでは、MORF システムが麻酔、蘇生、集中治療の最小限のモニタリングに関する基準を概説しました (161 年 2 月 24 日の No. 1997/DM-8「麻酔、蘇生、集中治療中の患者の安全を確保するための措置について」) )。データを表 9、表 XNUMX に示します。 表8 麻酔
表9 蘇生と集中治療の実施
効果的な集中治療を実施するには、心血管系、呼吸器系、神経系、肝臓の機能、腎臓、消化管、造血、止血、エネルギー、水電解質、酸塩基、腫瘍浸透を監視する必要があります。残高。 同様に重要なのは、進行中の治療介入とその結果を集中的に監視することです。 外部および内部の微生物学的状態を監視すること、および予後基準と結果評価を使用することが重要な役割を果たします。 まず第一に、患者の状態の臨床的評価と非侵襲的なモニタリング方法を使用する必要があります。 臨床モニタリング、つまり臨床徴候や症状の観察、定性的データは、高度な技術を使用して得られる定量的指標と同様に重要です。 システム機能の監視 循環器系のモニタリング 循環モニタリングは、心電図を使用して心不整脈と心筋虚血をタイムリーに検出します。 心不整脈は、四肢またはその変形からの標準誘導の誘導 V1 および V2 の心電図モニターの P 波および ORS 複合体によって識別できます。 心筋虚血は、ECGのSTセグメントの結果として生じる抑制によって識別できます。 1)胸部リードV5、およびその修正のXNUMXつ - 左側壁の中隔の虚血。 2)四肢からの標準2リード - 右冠状動脈の流域における心筋の基底領域の虚血。 下降する ST 低下 (上昇) は、ストレス誘発性虚血の指標です。 血行動態のモニタリングは、次の方法で実行されます。 1) 血圧測定; 2) 体積応力試験と組み合わせた CVP 測定 (これは血管充填に関する情報です)。 3) 浮遊肺動脈カテーテルを使用した肺動脈圧と楔圧 (PWP) の決定は、CVP よりも血管内容積を評価するためのより正確な方法であり、左心室前負荷の尺度としても機能します。 4)熱希釈法、フィック法(CO = VCO)を使用した心拍出量の決定2 /CaCO2)、ドップラー技術のさまざまな修正(食道ドップラー心エコー検査)、心臓の超音波検査。 呼吸モニタリング 呼吸モニタリングは、臨床症状とカプノグラフィー、パルスオキシメトリー、肺活量測定、および定期的な血液ガス検査のデータに従って実行されます。 人工呼吸中、「人工呼吸器 - 患者」システムの圧力と吸入混合気の酸素濃度 (FiO2). 呼吸不全の臨床徴候:頻繁な(成人の場合、毎分24〜30回以上)浅い呼吸、追加の筋肉(胸鎖乳突筋、腹部など)の呼吸への参加。鼻、強制的な半座位)、発汗、チアノーゼ、心拍数の変化(最初に増加し、次に不整脈が発生する可能性があります)および血圧(増加し、重度の低酸素症を伴う - 減少)、多幸感から意識の変化昏睡。 カプノグラフィーにより、換気障害のタイムリーな検出が可能になります。2 最後に吐き出された空気中 - FetCO2 > 6,4%)、過呼吸 (FetCO2 <4,9%)、不均一な換気(肺胞カプノグラムプラトーの傾斜角-5°)。 機械的人工呼吸中、カプノグラフがない場合、換気量は、呼気経路に設置された容積測定肺活量計を使用して測定された微小呼吸量(Vist。)によって制御されます。 さらに、吸入ガス混合物の酸素濃度を計算し、このシステムの気密性を判断するために必要な、微小吸気量(Vappar。)が監視されます-「人工呼吸器-患者」。 気密性の制御は、モノバキュメーターによって測定される「デバイスシック」システム内の圧力によっても達成されます。 パルスオキシメトリーにより、肺の酸素化障害、低酸素血症 (SaO2 < 94%。 さらに、プレチスモグラムの性質に基づいて、微小循環の状態と心拍出量を判断できます。 血液ガスの追加研究は、肺のガス交換障害の程度を評価するのに役立ちます(酸素分圧の肺胞動脈勾配の大きさによって。一部のモニターは、コンプライアンスに基づいて機械的換気中の呼吸の生体力学の評価を提供できます肺と胸部(C、通常60〜100 ml)および呼吸管の抵抗(抵抗)(R、通常2〜3 cm)。 神経機能のモニタリング 神経機能のモニタリングは、グラスゴースケールで意識を評価することによって行われます(刺激の増加に対する開眼反応、運動および言語反応に基づく:15ポイント - 正常、3ポイント - 脳死)。 さらに、頭蓋内圧および脳血流が決定される(例えば、経頭蓋ドップラーモニターを使用して)。 腎機能は、通常 0,5 ml/kg/h を超える XNUMX 時間ごとの尿量を測定することによって最も一般的に監視されます。 講義番号15.人工肺換気 人工肺換気 (ALV) は、周囲の空気 (またはガスの特定の混合物) と肺の肺胞との間のガス交換を提供し、麻酔の構成要素として、呼吸が突然停止した場合の蘇生手段として使用されます。また、急性呼吸不全、神経系および筋肉系のいくつかの疾患の集中治療の手段として。 人工肺換気 (ALV) の最新の方法は、単純なものとハードウェアに分けることができます。 機械的換気の簡単な方法は、通常、緊急事態(無呼吸、異常なリズムを伴う、苦痛な呼吸、低酸素血症および(または)高炭酸ガス血症の増加、および重度の代謝障害)で使用されます。 口から口へ、口から鼻へのIVL(人工呼吸)の呼気方法は簡単です。 必要に応じて、長期の機械的換気(50時間から数か月、さらには数年)にハードウェア方式が使用されます。 Phase-1人工呼吸器には大きな可能性があります。 小児科の診療のために、装置「Vita-12」が製造されています。 人工呼吸器は、気管内チューブまたは気管切開カニューレを介して患者の気道に接続されます。 ハードウェア換気は、20 分間に 1 ~ 60 サイクルの通常の頻度モードで実行されます。 実際には、高周波モード(1分間に150サイクル以上)の機械的換気があり、XNUMX回換気量が著しく減少し(最大XNUMXml以下)、吸気終了時の肺の陽圧が減少し、胸腔内圧だけでなく、心臓への血流も改善します。 また、高周波モードでは、呼吸器への患者の適応が促進されます。 高周波換気には、容積換気、振動換気、ジェット換気の 80 つの方法があります。 ボリュームは、通常、100 分あたり 1-600 の呼吸数、振動 IVL - 3600 分あたり 1-100 の呼吸数で実行され、連続的または断続的なガス流の振動を保証します。 直径 300 ~ 1 の針またはカテーテルを通して 2 ~ 2 気圧の圧力で酸素のジェットを気道に吹き込む、4 分間に XNUMX ~ XNUMX 回の呼吸数を持つ最も普及しているジェット高周波換気んん。 ジェット換気は、気管内チューブまたは気管切開術(同時に大気が気道に吸い込まれる)と、鼻腔または経皮的に気管に挿入されるカテーテル(穿刺)を介して行われます。 後者は、気管挿管の条件がない状況で重要です。 肺の人工換気は自動モードで実行できますが、これは、患者の自発呼吸が完全に欠如している場合、または薬理学的薬物(筋弛緩薬)によって抑制されている場合に許容されます。 補助換気も行われますが、この場合、患者の独立した呼吸が維持されます。 ガスは、患者が弱い吸入を試みた後、または患者がデバイスの個別に選択された操作モードに同期した後に供給されます。 間欠的強制換気(PMV)モードもあります。これは、機械的換気から自発呼吸への段階的な移行中に適用されます。 この場合、患者は自分で呼吸しますが、さらに、ガス混合物の連続的な流れが気道に供給されます。 この背景に対して、指定された頻度(10分あたり1〜10回)で、デバイスは、患者の独立したインスピレーションと一致する(同期されたPVL)または一致しない(同期されていないPVL)人工呼吸を実行します。 人工呼吸を徐々に減らすことで、患者が自発呼吸できるように準備することができます。 呼吸回路を表XNUMXに示します。 表10 呼吸回路
バッグまたはマスクを使用した手動換気は容易に利用でき、多くの場合、肺を適切に膨らませるのに十分です。 その成功は、原則として、肺の病理の重症度ではなく、マスクのサイズの正しい選択とオペレーターの経験によって決まります。 適応症 1.その後の挿管のための短期間の患者の蘇生と準備。 2. 抜管後の無気肺を防ぐためのバッグとマスクによる定期的な換気。 3.バッグとマスクによる換気の制限。 機器 従来の呼吸バッグと、圧力計が取り付けられたマスク、または酸素チャンバーを備えた自動膨張式呼吸バッグが使用されます。 のテクニック 1.マスクを患者の顔にしっかりと置き、指で顎を固定して患者の頭を正中位置にする必要があります。 マスクは目の上にあってはいけません。 2. 呼吸数 - 通常、30 分間に 50 ~ 1 回。 3. 吸気圧 - 通常 20 ~ 30 cm の水圧。 美術。 4. 女性の陣痛活動における一次蘇生中は、より高い圧力 (水柱 30 ~ 60 cm) が許容されます。 有効性の評価 1.心拍数が正常な数値に戻り、中枢性チアノーゼが消失します。 2.胸部の可動域は良好である必要があり、呼吸は両側で等しくうまく行われます。 3.血液のガス組成の研究は通常必要であり、長時間の蘇生中に実施されます。 合併症 1.気胸。 2. 膨満感。 3. 低換気症候群または無呼吸のエピソード。 4.顔の皮膚の刺激。 5. 網膜剥離(眼にマスクを装着し、長期的に高いピーク圧を発生させた場合)。 6. マスクとバッグの換気は、患者が積極的に抵抗する場合、患者の状態を悪化させる可能性があります。 ハードウェア IVL 適応症 1.無呼吸。 2. 呼吸不全の徴候がなくても、急性期の昏睡。 3.標準的な抗けいれん薬療法によって制御されない発作。 4. 病因によるショック。 5.過呼吸症候群におけるCNS抑制症候群のダイナミクスの増加。 6.新生児の出生時脊椎損傷 - 息切れを背景に、強制呼吸と広範囲の喘鳴の出現。 7. RO2 50mmHg未満の毛細血管血。 美術。 FiOとの混合物による自発呼吸中2 0,6以上。 8.RSO2 毛細血管血が60mmHg以上。 美術。 または35mmHg未満。 美術。 自発呼吸で。 装備:「PHASE-5」「BP-2001」「インファントスター100or200」「セクリスト100or200」「ベイビーログ1」「ステファン」など 治療の原則 1. 硬直した肺の酸素化は、吸気酸素濃度の増加、吸気圧の増加、PEEP の増加、吸気時間の延長、プラトー圧の増加によって達成できます。 2.換気(COの除去)2)一回換気量の増加、頻度の増加、および呼気時間の延長によって強化することができます。 3.換気パラメータ(頻度、吸気圧、吸気プラトー、吸気-呼気比、PEEP)の選択は、基礎疾患の性質と治療に対する患者の反応によって異なります。 IVLの目的 1.酸素:pOに達する2 50~100mmHg 美術。 2.pCOをホールド2 35-45 mm Hg 以内。 美術。 3. 例外: 場合によっては、pO インジケーター2 とpCO2 上記とは異なる場合があります。 1) 慢性肺病変では、より高い pCO 値2 ポータブル; 2) 重度の心臓障害がある場合、より小さな pO 値が許容されます2; 3)肺高血圧症の場合の治療アプローチに応じて、より大きなまたはより小さなpCO値が許容されます2. 4. 適応と換気パラメータは常に文書化する必要があります。 のテクニック 1. IVL の初期パラメータ: 吸気圧 20 ~ 24 cm の水圧。 美術。; 4〜6cmの水からPEER。 美術。; 16分あたりの呼吸数24〜1、吸入時間0,4〜0,6秒、DO 6〜10リットル/分、MOV(分換気量)450〜600ml /分。 2.人工呼吸器との同期。 原則として、患者は人工呼吸器と同期しています。 しかし、興奮は同期を損なう可能性があります。そのような場合、薬物療法(モルヒネ、プロメドール、オキシ酪酸ナトリウム、筋弛緩薬)が必要になる場合があります。 調査 1. 調査の重要な構成要素は、繰り返される血液ガス検査です。 2.身体検査。 IVL の妥当性の管理。 簡単な方法で緊急換気を行う場合、患者の皮膚の色と胸の動きを観察するだけで十分です。 胸壁は吸気ごとに拡張し、呼気ごとに下がるはずですが、上腹部が上昇すると、吹き出された空気が食道と胃に入ります。 その理由は、多くの場合、患者の頭の位置が間違っていることです。 長期の人工呼吸を行う場合、その妥当性を判断する必要があります。 患者の自発呼吸が薬理学的製剤によって抑制されていない場合、実行されたIVLの妥当性の主な兆候のXNUMXつは、患者が人工呼吸器にうまく適応していることです。 明確な意識がある場合、患者は空気不足や不快感を感じてはなりません。 肺の呼吸音は両側で同じでなければならず、皮膚の色は正常でなければなりません。 合併症 1. 人工呼吸器の最も一般的な合併症は、間質性肺気腫、気胸、気縦隔炎の発症を伴う肺胞の破裂です。 2. その他の合併症には、細菌汚染と感染、気管内チューブの閉塞または抜管、片肺挿管、心タンポナーデを伴う心膜炎、静脈還流の減少と心拍出量の減少、肺のプロセスの慢性化、狭窄と閉塞があります。気管。 機械的換気の背景に対して、自発呼吸の条件下での導入は低酸素血症を伴うであろう用量で十分なレベルと深さの麻酔を提供するはずの多くの鎮痛剤を使用することが可能です。 血液への酸素の良好な供給を維持することにより、機械的換気は、体が外科的損傷に対処することに貢献します。 胸部の臓器(肺、食道)の多くの手術では、別の気管支挿管が使用されます。これにより、外科医の作業を容易にするために、外科的介入中に片方の肺の換気をオフにすることができます。 この挿管は、手術した肺の内容物が健康な肺に漏れるのも防ぎます。 喉頭と気道の手術中は、経カテーテルジェット高周波換気が使用されます。これにより、手術野の検査が容易になり、気管と気管支を開いた状態で適切なガス交換を維持できます。 全身麻酔と筋肉弛緩の条件下では、患者は結果として生じる低酸素症と低換気に反応することができません。したがって、経皮的手段によって血液ガス含有量を制御することが重要です(酸素分圧と二酸化炭素分圧の継続的な監視)。特殊なセンサーを使用。 臨床死または苦痛の場合、機械的人工呼吸は蘇生の必須の要素です。 意識が完全に回復し、自発呼吸が完了した後にのみ、IVLの実行を停止することができます。 集中治療室では、人工呼吸器が急性呼吸不全の治療に最も効果的な方法です。 それは、下部鼻腔または気管切開を通して気管に挿入されるチューブを通して行われます。 特に重要なのは、気道のケア、適切な排水です。 補助人工呼吸器は、慢性呼吸不全の患者を治療するために 30 ~ 40 分間のセッションで使用されます。 IVLは、昏睡状態(外傷、脳外科手術)の患者、および呼吸筋の末梢損傷(多発根神経炎、脊髄損傷、筋萎縮性側索硬化症)の患者に使用されます。 ALVは、胸部外傷、さまざまな中毒、脳血管障害、破傷風、ボツリヌス中毒の患者の治療にも広く使用されています。 講義第16号。点滴療法。 輸液療法は、体の水 - 電解質、酸 - 塩基のバランスを正常化するため、および強制利尿(利尿薬と組み合わせて)するために、静脈内または皮膚の下に薬物および体液を点滴または注入することです。 輸液療法の適応症:すべてのタイプのショック、失血、血液量減少、不屈の嘔吐、激しい下痢、水分摂取の拒否、火傷、腎臓病の結果としての水分、電解質およびタンパク質の喪失。 塩基性イオン(ナトリウム、カリウム、塩素など)の含有量の違反、アシドーシス、アルカローシスおよび中毒。 体の脱水の主な兆候:眼球の眼窩への収縮、鈍い角膜、乾燥した、弾力性のない皮膚、特徴的な動悸、乏尿、尿が濃縮されて濃い黄色になり、全身状態が落ち込んでいます。 点滴療法の禁忌は、急性心血管不全、肺水腫、無尿です。 クリスタロイド溶液は、水分と電解質の欠乏を補うことができます。 0,85% 塩化ナトリウム溶液、リンガーおよびリンガーロック溶液、5% 塩化ナトリウム溶液、5-40% グルコース溶液およびその他の溶液を適用します。 それらは、10~50ml/kg以上の容量で、静脈内および皮下に、ストリーム(重度の脱水を伴う)および点滴によって投与される。 これらの解決策は、過剰摂取を除いて合併症を引き起こしません。 注入療法の目標は、BCCの回復、循環血液量減少の排除、適切な心拍出量の確保、正常な血漿浸透圧の維持と回復、適切な微小循環の確保、血球の凝集の防止、血液の酸素輸送機能の正常化です。 コロイド溶液は高分子物質の溶液です。 それらは血管床の液体の保持に貢献します。 ヘモデズ、ポリグルシン、レオポリグルユキン、レオグルマンが使用されます。 それらの導入により、アレルギーまたは発熱反応の形で現れる合併症が発生する可能性があります。 投与経路-静脈内投与、皮下投与の頻度は低く、点滴。 30日量は40〜XNUMXml/kgを超えません。 彼らは解毒の品質を持っています。 非経口栄養源として、長期にわたる食事の拒否や口からの摂食ができない場合に使用されます。 血液およびカゼイン加水分解物が使用されます(アルベジンネオ、ポリアミン、リポファンジンなど)。 それらはアミノ酸、脂質およびブドウ糖を含んでいます。 時々、導入に対するアレルギー反応があります。 注入の速度と量。 容量注入速度に関するすべての注入は、BCC 欠乏症の迅速な修正を必要とする場合と必要としない場合の XNUMX つのカテゴリに分けることができます。 主な問題は、血液量減少症の迅速な除去が必要な患者である可能性があります。 つまり、血液循環を大幅に集中化することなく、臓器や組織の局所灌流を適切に供給するために、注入速度とその量は心臓の性能を確保する必要があります。 最初は健康な心臓を持つ患者では、60 つの臨床的ランドマークが最も有益です: 平均血圧 > 2 mm Hg。 美術。; 中心静脈圧 - CVP> 50 cm の水。 美術。; 利尿 15 ml/h。 疑わしい場合には、負荷をかけて試験を実施します。20〜400mlのクリスタロイド溶液を500〜XNUMX分間かけて注ぎ、CVPと利尿の動態を観察します。 利尿の増加を伴わない CVP の有意な上昇は心不全を示している可能性があり、これは血行動態を評価するためのより複雑で有益な方法の必要性を示唆しています。 両方の値を低く保つことは血液量減少を示唆し、段階的な評価を繰り返して高い注入速度を維持します。 利尿の増加は、腎前乏尿(循環血液量減少に起因する腎臓の低灌流)を示します。 循環不全患者の輸液療法には、血行動態、大規模かつ特別な監視モニタリングに関する明確な知識が必要です。 デキストランはコロイド血漿代用物であり、BCC の迅速な回復に非常に効果的です。 デキストランは、虚血性疾患および再灌流に対する特定の保護特性を備えており、そのリスクは主要な外科的介入中に常に存在します。 デキストランのマイナス面には、かなりの量の薬物(> 20 ml / kg)を使用する必要がある場合の血小板の分解(特にレオポリグルシンの特徴)による出血のリスク、および薬物の抗原特性の一時的な変化が含まれます。血液。 デキストランは、腎臓の尿細管の上皮の「火傷」を引き起こす能力があるため危険であり、したがって腎虚血および腎不全には禁忌です. 彼らはしばしばアナフィラキシー反応を引き起こし、それは非常に深刻な場合があります. 特に興味深いのは、血漿代替物の天然コロイドであるため、ヒトアルブミンの溶液です。 内皮の損傷を伴う多くの重篤な状態 (主にあらゆる種類の全身性炎症性疾患) では、アルブミンが血管外層の細胞間スペースに入り込み、水を引き寄せて間質組織の浮腫 (主に肺) を悪化させます。 新鮮凍結血漿は、単一のドナーから採取された製品です。 FFP は全血から分離され、採血後 6 時間以内に直ちに凍結されます。 ビニール袋に入れて30℃で1年間保存。 凝固因子は不安定であるため、FFP は 2°C で急速解凍後、最初の 37 時間以内に注入する必要があります。 新鮮凍結血漿(FFP)の輸血は、HIV、B型およびC型肝炎などの危険な感染症にかかるリスクが高くなります.FFPの輸血中のアナフィラキシーおよび発熱反応の頻度は非常に高いため、ABOシステムによる適合性考慮する必要があります。 若い女性の場合は、Rh 適合性を考慮する必要があります。 現在、FFPの使用の唯一の絶対的な適応症は、凝固障害性出血の予防と治療です。 FFPは、止血と膠質浸透圧の維持というXNUMXつの重要な機能を同時に実行します。 FFPはまた、凝固低下、間接抗凝固薬の過剰摂取、治療的血漿交換、急性DIC、および血液凝固因子の欠乏に関連する遺伝性疾患で輸血されます。 適切な治療の指標は、患者の明確な意識、温かい皮膚、安定した血行動態、重度の頻脈と息切れの欠如、十分な利尿 - 30-40 ml/h 以内です。 1. 輸血 輸血の合併症:血液凝固系の輸血後障害、高熱症候群および心血管代償不全の存在を伴う重度の発熱性反応、アナフィラキシー反応、赤血球溶血、急性腎不全など。 ほとんどの合併症の基礎は、異物組織による拒絶反応です。 輸血後の反応や合併症のリスクが大きいため、缶詰の全血の輸血の適応はありませんが、最も危険なのはレシピエントの感染のリスクが高いことです. 外科的介入中の急性失血およびBCC欠乏症の適切な補充の場合、麻酔下の酸素消費量が大幅に減少し、追加の酸素化が許容されるため、ヘモグロビンとヘマトクリットの急激な減少でさえ患者の生命を脅かすことはなく、血液希釈が役立ちます微小血栓症の発生とデポからの赤血球の動員を防ぎ、血流速度を高めます。人が本来持っている赤血球の「予備」は、特に患者がいる安静状態では、実際のニーズを大幅に超えています。現時点では。 手術中にドナーの血液と赤血球の輸血を処方するための推奨事項。 1. BCCの回復後に赤血球塊の輸血が行われます。 2.死に至る可能性のある重度の付随する病状がある場合(たとえば、重度の貧血は重度の冠状動脈性心臓病では許容されません)。 3.患者の赤血球の次の指標の存在下:ヘモグロビンで70〜80 g / l、ヘマトクリットで25%、赤血球の数は2,5万です。 輸血の適応症は、出血と止血の修正です。 赤血球の種類:全血、赤血球塊、EMOL(白血球から分離された赤血球塊、生理食塩水を含む血小板)。 血液は、使い捨てシステムを使用して、毎分60~100滴の速度で30~50ml/kgの量で点滴により静脈内投与される。 輸血の前に、レシピエントとドナーの血液型とRh因子を決定し、それらの適合性についてテストを実施し、適合性についての生物学的テストを患者のベッドサイドで実行する必要があります。 アナフィラキシー反応が起こると、輸血が中止され、ショックを取り除くための措置が開始されます。 標準的な濃縮血小板は、0,5 回遠心分離された血小板の懸濁液です。最小血小板数は1012リットルあたり0,2×109、白血球はXNUMXリットルあたりXNUMX×XNUMXです。 止血特性と生存率は、準備の次の12〜24時間で最も顕著になりますが、薬剤は採血の瞬間から3〜5日以内に使用できます。 血小板濃縮物は、血小板減少症(白血病、骨髄形成不全)、出血性症候群を伴う血栓症に使用されます。 2. 静脈栄養 恒常性の深刻な障害を伴う重度の疾患では、体にエネルギーとプラスチック材料を提供する必要があります。 したがって、何らかの理由で口からの栄養が損なわれたり、完全に不可能になったりした場合は、患者を非経口栄養に移行させる必要があります。 さまざまな病因の危機的な状況では、タンパク質代謝に最も重要な変化が起こります-特に横紋筋で集中的なタンパク質分解が観察されます。 進行中のプロセスの重症度に応じて、体タンパク質は 75 日あたり 150 ~ 11 g の量で異化されます (毎日のタンパク質損失は表 XNUMX に示されています)。 これは、糖新生の過程でエネルギー源として使用される必須アミノ酸の欠乏につながり、負の窒素バランスをもたらします. 表11 危機的状況での毎日のタンパク質損失
窒素の損失は体重の減少につながります。これは、窒素1 g \u6,25d 25 gのタンパク質(アミノ酸)\uXNUMXd XNUMX gの筋肉組織だからです。 重大な状態の発症から XNUMX 日以内に、十分な量の必須栄養素を導入する適切な治療を行わないと、それ自体の炭水化物の蓄えが使い果たされ、体はタンパク質と脂肪からエネルギーを受け取ります。 この点で、代謝プロセスの量的変化だけでなく質的変化も行われます。 非経口栄養の主な適応症は次のとおりです。 1)胃腸管の発達の異常(食道閉鎖症、幽門狭窄症など、術前および術後の期間); 2)口腔および咽頭の火傷および損傷; 3)広範囲の体の火傷; 4) 腹膜炎; 5) 麻痺性イレウス; 6) 高腸瘻; 7)不屈の嘔吐; 8) 昏睡; 9) 異化プロセスの増加および非代償性代謝障害を伴う重篤な疾患(敗血症、重篤な肺炎)。 10)萎縮およびジストロフィー。 11)神経症による食欲不振。 非経口栄養は、大量摂取、水電解質障害、微小循環障害の排除、低酸素血症、および代謝性アシドーシスの代償状態で実施する必要があります。 非経口栄養の基本原則は、体に十分な量のエネルギーとタンパク質を提供することです。 非経口栄養の目的で、次の溶液が使用されます。 炭水化物:あらゆる年齢で使用される最も受け入れられる薬はブドウ糖です。 毎日の食事に含まれる炭水化物の比率は、少なくとも50〜60%である必要があります。 完全に利用するには、投与速度を維持する必要があります。ブドウ糖には、1gあたり4単位のインスリン、カリウム、エネルギー利用に関与する補酵素:ピリドキサールリン酸、コカルボキシラーゼ、リポ酸、ATPなどの成分を供給する必要があります-0,5-1静脈内にXNUMX日あたりmg/kg。 適切に投与された場合、高濃度のグルコースは浸透圧利尿や血糖値の大幅な上昇を引き起こしません. 窒素栄養には、高品質のタンパク質加水分解物(アミノソール、アミノン)または結晶性アミノ酸の溶液が使用されます. これらの薬は、必須アミノ酸と非必須アミノ酸をうまく組み合わせており、毒性が低く、アレルギー反応を引き起こすことはめったにありません. 投与されるタンパク質調製物の用量は、タンパク質代謝の違反の程度に依存します。 代償性障害の場合、投与されるタンパク質の用量は、1日あたり3g/kg体重です。 低タンパク血症、アルブミン-グロブリン比の減少、毎日の尿中の尿素の増加によって現れるタンパク質代謝の補償解除には、タンパク質の用量の増加(4日あたり25〜1g / kg)および抗異化療法の導入が必要です。 これには、同化ホルモン(レタボリル、ネラボリル-5 mgを7〜140日に筋肉内に150回)、高カロリー輸液モード(1000〜5 kcal / kg体重/日)での非経口栄養プログラムの構築、プロテアーゼ阻害剤(kontrykal、trasylol)が含まれます。 7 U / kg /日、200〜220日間)。 プラスチック材料を適切に吸収するには、導入された窒素の各グラムにXNUMX〜XNUMXkcalを供給する必要があります。 アミノ酸溶液は有毒な混合物を形成するため、濃縮グルコース溶液と一緒に投与しないでください。 アミノ酸の導入に対する相対的禁忌:腎不全および肝不全、ショックおよび低酸素症。 ポリ不飽和脂肪酸を含む脂肪乳剤は、脂肪代謝を修正し、非経口栄養のカロリー量を増やすために使用されます。 脂肪は最も高カロリーの製品ですが、その利用のためには、最適な用量と投与速度を維持する必要があります。 脂肪乳剤は、濃縮ポリイオングルコース溶液と一緒に、およびそれらの前後に投与しないでください。 脂肪乳剤の導入に関する禁忌:肝不全、脂肪血症、低酸素血症、ショック状態、血栓出血性症候群、微小循環障害、脳浮腫、出血性素因。 非経口栄養に必要な主成分のデータを表12と表13に示します。 表12 非経口栄養の主要成分の投与量、割合、カロリー量
非経口栄養を処方するときは、エネルギー利用反応の補酵素である、多くの代謝プロセスに関与するビタミンの最適な用量を導入する必要があります。 表13 非経口栄養中に必要なビタミンの用量 (100 kcal あたりの mg)
どのモードでも実行される非経口栄養のプログラムは、成分のバランスの取れた比率に関して作成する必要があります。 タンパク質、脂肪、炭水化物の最適な比率は 1:1,8:5,6 です。 合成の過程でタンパク質、脂肪、炭水化物を分解して含めるには、一定量の水が必要です。 水の必要量と食物のカロリー量の比率は 1 ml H2○~1kcal(1: 1)。 Harris-Benedict による安静時の必要エネルギー消費量 (ERP) の計算: 男性 - EZP = 66,5 + 13,7 x 体重、kg + 5 x 身長、cm - 6,8 x 年齢 (歳)。 女性 - EZP = 66,5 + 9,6 x 体重 kg + 1,8 x 身長 cm - 4,7 x 年齢 (歳)。 ハリス・ベネディクト式によって決定される EZP 値は、25 日あたり平均 14 kcal/kg です。 計算後、患者の身体活動係数 (PFA)、臨床状態に基づいた代謝活動係数 (FMA)、および体温係数 (TF) が選択され、特定の患者のエネルギー必要量 (E) が決定されます。患者様が決まります。 FFA、FMA、および TF を計算するための係数を表 XNUMX に示します。 表14 FFA、FMA、TF を計算するための係数
毎日の PE を決定するには、EZP 値に FFA、FMA、および TF を掛けます。 3.解毒療法 重度の中毒では、体から毒素を結合して除去することを目的とした積極的な解毒療法が必要です。 この目的のために、ポリビニルピロリドン(ネオコンペンサン、ジェモデス)とゼラチノールの溶液が最も頻繁に使用され、毒素を吸着および中和し、その後腎臓から排泄されます。 これらの溶液は、患者の体重1kg当たり5~10mlの量で滴下投与され、ビタミンCおよび塩化カリウム溶液が体重1kg当たり1ミリモルの最小量で加えられる。 効果的な抗低酸素剤および抗酸化剤であるマフソールには、顕著な解毒特性もあります。 さらに、血液の微小循環とレオロジー特性を改善し、解毒効果にも貢献します。 さまざまな中毒で、解毒の最も効果的な方法の5つは強制利尿です。 強制利尿を目的とした静脈内輸液は、重度の中毒と、患者が飲酒を拒否した軽度の中毒に対して処方されます。 強制利尿の禁忌は、急性心血管不全および急性腎不全(無尿)です。 強制利尿を行うには、注入された液体の量と定量的組成の厳密な説明、利尿薬のタイムリーな任命、明確な臨床的および生化学的管理が必要です。 水負荷の主な解決策として、次のものが提案されています。グルコース14,5 g。 塩化ナトリウム1,2g; 重炭酸ナトリウム2,0g; 塩化カリウム 2,2g; 1000mlまでの蒸留水。 この溶液は等張であり、必要量の重炭酸ナトリウムを含み、その中のカリウム濃度は許容値を超えず、グルコースと塩の浸透圧濃度の比率は2:1です。 強制利尿の初期段階では、血漿代替および解毒溶液を導入することもお勧めします。インフコール 8-10 ml/kg kg、レオポリグリキン 15-20 ml/kg。 注入された溶液の総量は、毎日の必要量の約 1,5 倍を超える必要があります。 著者: Kolesnikova M.A.
タッチエミュレーション用人工皮革
15.04.2024 Petgugu グローバル猫砂
15.04.2024 思いやりのある男性の魅力
14.04.2024
▪ 記事 バロメーターとして機能する植物はどれですか? 詳細な回答 ▪ 記事 7 MHz のアンテナ グラウンド プレーン。 無線エレクトロニクスと電気工学の百科事典
ホームページ | 図書館 | 物品 | サイトマップ | サイトレビュー www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese

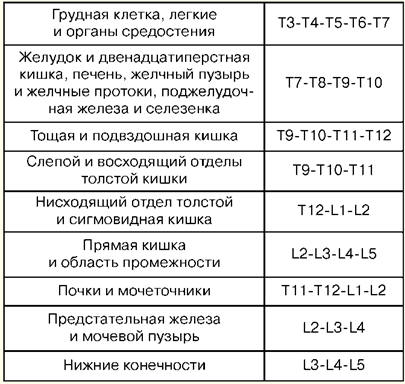




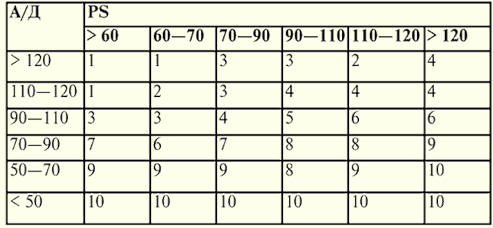




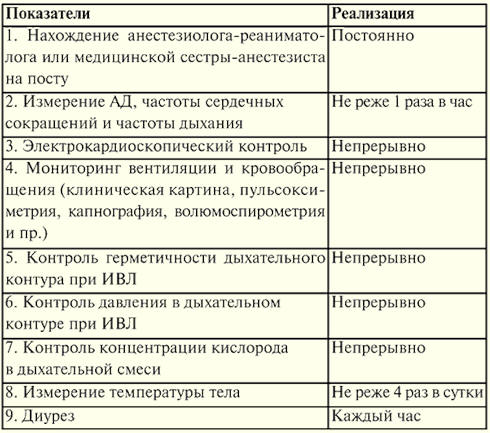


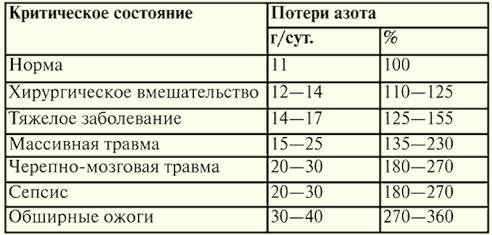

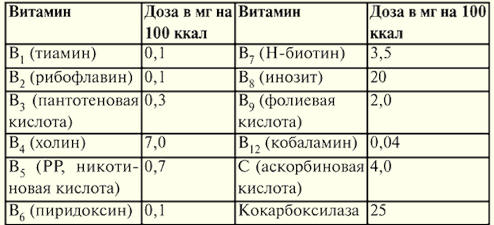

 他の記事も見る セクション
他の記事も見る セクション 